题目内容
6.如图是实验室常见的制取气体的装置: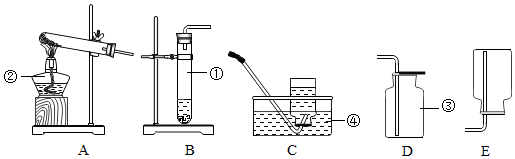
(1)写出仪器名称:①试管,②酒精灯,③集气瓶,④水槽.
(2)实验室采用装置A制取氧气时,其试管中应放的药品是高锰酸钾,试管口还要放一团棉花,目的是防止加热时高锰酸钾粉末进入导管.
(3)采用装置B制取氧气时,其试管中应放的药品是过氧化氢、二氧化锰,所发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)收集氧气可以选择装置C或D,原因是氧气不易溶于水,氧气密度比空气大.
(5)某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作会引起什么后果水槽中的水倒吸入热的试管,引起试管炸裂
(6)以下是实验步骤,将步骤的序号按正确的先后次序排列为BDFAEGC.
A、点燃酒精灯加热 B、检查气密性 C、熄灭酒精灯 D、向试管中装入药品
E、收集气体 F、将试管固定在铁架台上 G、从水中撤离导管.
分析 (1)据常用仪器回答;
(2)据高锰酸钾制取氧气的注意事项分析解答;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(4)氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;
(5)据高锰酸钾注意事项解答;
(6)据制取氧气的实验步骤分析解答.
解答 解:(1)标号仪器分别是试管、酒精灯、集气瓶、水槽;
(2)加热高锰酸钾时试管口要放一团棉花,是为了防止加热时高锰酸钾粉末进入导管,根据下面的空可知试管内放的是高锰酸钾;
(3)采用装置B制取氧气时,说明是在常温下用过氧化氢溶液和二氧化锰制取氧气,二氧化锰在此反应中起催化作用,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;
(5)收集完毕,先停止加热再将导管移出水面,是为了防止水槽中水倒吸入热的试管,引起试管炸裂;
(6)加热高锰酸钾制取氧气的实验步骤是:检查气密性,加入药品并固定,然后点燃酒精灯进行加热,收集气体,收集完毕先移导管后熄灯;
故答案为:(1)试管;酒精灯;集气瓶;水槽;
(2)高锰酸钾;防止加热时高锰酸钾粉末进入导管;
(3)过氧化氢、二氧化锰;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)C;D;氧气不易溶于水,氧气密度比空气大;
(5)水槽中的水倒吸入热的试管,引起试管炸裂;
(6)BDFAEGC.
点评 本题综合考查了仪器的用途、化学方程式的书写、装置选择、实验基本操作、步骤等知识,只有综合理解化学知识才能够正确的解答.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
16.生产自来水的时,向水中通入一定量的氯气.这是因为氯气跟水反应,生成盐酸和次氯酸,其中次氯酸具有强氧化性,可以起到消毒灭菌的作用.某学生用这种自来水来配制下列物质的溶液.通常不会使药品明显变质的是( )
| A. | 石蕊试液 | B. | 硝酸银溶液 | C. | 碳酸钠溶液 | D. | 硝酸钾溶液 |
11.区分如表各组物质所用的两种方法都正确的是( )
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 氮气和二氧化碳 | 分别通入澄清石灰水 | 分别通入石蕊溶液 |
| B | 碳酸钠溶液与硫酸钠溶液 | 加硝酸钡溶液 | 加稀盐酸 |
| C | 碳酸氢铵与硫酸钾 | 取样品闻气味 | 观察颜色 |
| D | 棉布与涤纶布 | 取样品点燃闻气味 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
15.新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下:MFe2Ox$→_{SO_{2}}^{常温下}$MFe2Oy,则下列判断正确的是( )
| A. | MFe2Ox是还原剂 | B. | SO2是该反应的催化剂 | ||
| C. | x<y | D. | SO2发生了分解反应 |

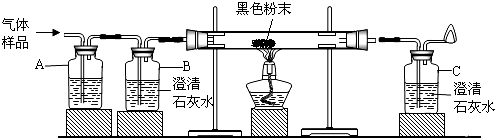
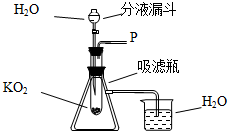 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.