题目内容
实验室中用氯酸钾和二氧化锰制取氧气一段时间后冷却至室温,称量所得固体质量为10g.若剩余固体中氯元素的质量分数为14.2%,则剩余混合物中钾元素的质量分数为 .
考点:元素的质量分数计算
专题:化学式的计算
分析:根据氯酸钾、氯化钾中钾元素和氯元素的质量比分析计算.
解答:解:氯酸钾在二氧化锰的催化作用、加热条件下生成氯化钾和氧气,氯酸钾、氯化钾 的化学式分别是:KClO3和KCl,加热一段时间后冷却至室温,氯酸钾可能未完全分解,但无论是氯酸钾、还是氯化钾,钾元素和氯元素的质量比始终是39:35.5;
由题意可知:称量所得固体质量为10g.若剩余固体中氯元素的质量分数为14.2%,则氯元素的质量是10g×14.2%=1.42g,设钾元素的质量是x,则
=
,解得x=
,则剩余混合物中钾元素的质量分数为:
×100%=15.6%;
故答案为:15.6%.
由题意可知:称量所得固体质量为10g.若剩余固体中氯元素的质量分数为14.2%,则氯元素的质量是10g×14.2%=1.42g,设钾元素的质量是x,则
| 39 |
| 35.5 |
| x |
| 1.42g |
| 1.56g |
| 10g |
| 1.56g |
| 10g |
故答案为:15.6%.
点评:了解氯酸钾、氯化钾的化学式,并能据化学式特点灵活分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途主要是由其化学性质决定的是( )
| A、用铜丝做导线 |
| B、用铁锅做炊具 |
| C、用煤作燃料 |
| D、发烧病人用酒精擦身体降温 |
下列实验能够直接用于验证质量守恒定律的是( )
A、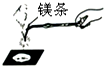 |
B、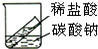 |
C、 |
D、 |
下列说法完全正确的是( )
| A、铁--由分子构成,二氧化碳--由原子构成,氯化钠--由离子构成 |
| B、分子--化学变化中的最小粒子,原子--保持物质化学性质的最小粒子,离子--带电的原子 |
| C、Ar:表示氩气、氩元素和一个氩原子 |
| D、决定元素种类--最外层电子数 决定元素的化学性质--质子数,决定元素周期表元素排列顺序--质子数 |
对于盐酸,下列说法错误的是( )
| A、它是一种挥发性酸 |
| B、工业上用的盐酸往往带黄色 |
| C、它是氯化氢的水溶液 |
| D、紫色石蕊使盐酸变蓝色 |