题目内容
某化学兴趣小组在学习二氧化碳的性质时,进行如下探究实验,他们将在空气中燃烧的金属钠用燃烧匙放入装满二氧化碳的集气瓶中,发现金属钠依然剧烈燃烧,且在瓶壁和瓶底出现少量黑色固体和白色固体,请你一起参与他们的活动.
【提出问题】瓶底和瓶壁的白色固体的成分是什么?
【猜想与假设】根据化学反应前后元素种类不变,两位同学提出以下猜想:
猜想一:甲同学:“白色固体是氢氧化钠(NaOH)”;
猜想二:乙同学:“白色固体是碳酸钠(Na2CO3)”.
【实验与结论】
(1)甲同学的猜想一提出就遭到其他同学的反对,原因是 ;
(2)为了验证自己的猜想,乙同学设计了以下方案并实验验证:
(3)根据质量守恒定律,可推断出瓶中出现的黑色固体是 (填名称);根据以上实验探究内容,写出金属钠在二氧化碳中燃烧的化学方程式 ,该反应属于 (填基本类型).
(4)通过该实验探究,你对燃烧的新认识是 .
【提出问题】瓶底和瓶壁的白色固体的成分是什么?
【猜想与假设】根据化学反应前后元素种类不变,两位同学提出以下猜想:
猜想一:甲同学:“白色固体是氢氧化钠(NaOH)”;
猜想二:乙同学:“白色固体是碳酸钠(Na2CO3)”.
【实验与结论】
(1)甲同学的猜想一提出就遭到其他同学的反对,原因是
(2)为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量白色固体样品于试 管中,加入适量 观察现象 | 试管中产 生大量气泡 |
(4)通过该实验探究,你对燃烧的新认识是
考点:实验探究物质的组成成分以及含量,证明碳酸盐,反应类型的判定,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:科学探究
分析:根据实验现象考虑能否支持燃烧;根据实验注意事项分析燃酒精灯前,先向玻璃管中通会二氧化碳的目;根据质量守恒定律推测所含成分和元素;根据实验过程分析实验现象.根据化学方程式的书写方法分析.
解答:解:
【实验与结论】
(1)根据题意“金属钠用燃烧匙放入装满二氧化碳的集气瓶中,发现金属钠依然剧烈燃烧,且在瓶壁和瓶底出现少量黑色固体和白色固体”,则甲同学的猜想一提出就遭到其他同学的反对,原因是 根据质量守恒定律,反应物Na与CO2中不含氢元素;
(2)因为稀盐酸与碳酸钠反应生成二氧化碳气体,故设计实验:
(3)根据质量守恒定律的元素守恒,则可推断出瓶中出现的黑色固体是碳;根据以上实验探究内容,金属钠在二氧化碳中燃烧的化学方程式为4Na+3CO2
2Na2CO3+C,该反应符合“单+化=单+化”的特点,属于置换反应.
(4)通过该实验探究,对燃烧的新认识是燃烧不一定需要氧气.
故答案为:
(1)根据质量守恒定律,反应物Na与CO2中不含氢元素;
(2)
(3)碳; 4Na+3CO2
2Na2CO3+C,置换反应.
(4)燃烧不一定需要氧气.
【实验与结论】
(1)根据题意“金属钠用燃烧匙放入装满二氧化碳的集气瓶中,发现金属钠依然剧烈燃烧,且在瓶壁和瓶底出现少量黑色固体和白色固体”,则甲同学的猜想一提出就遭到其他同学的反对,原因是 根据质量守恒定律,反应物Na与CO2中不含氢元素;
(2)因为稀盐酸与碳酸钠反应生成二氧化碳气体,故设计实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量白色固体样品于试 管中,加入适量 稀盐酸, 观察现象 | 试管中产 生大量气泡 | 白色固体是碳酸钠(Na2CO3) |
| ||
(4)通过该实验探究,对燃烧的新认识是燃烧不一定需要氧气.
故答案为:
(1)根据质量守恒定律,反应物Na与CO2中不含氢元素;
(2)
| 实验步骤 | 实验现象 | 实验结论 |
| 稀盐酸, | 白色固体是碳酸钠(Na2CO3) |
| ||
(4)燃烧不一定需要氧气.
点评:本题属于信息题的考查,可以依据题目提供的信息结合二氧化碳的化学性质、质量守恒定律的运用等相关的知识进行分析得出结论,掌握反应现象与本质的联系;学会利用猜想和实验验证的方法,进行探究物质的组成成分以及含量.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
1个CO2分子和2个CO分子里含有一样多的是( )
| A、氧原子个数 | B、氧分子个数 |
| C、氧元素 | D、碳原子个数 |
在实验室制取氧气和验证氧气性质的实验中,正确操作是( )
| A、装药品前检查装置的气密性 |
| B、加热有气体产生就立即收集 |
| C、用带火星的木条伸入集气瓶中检验氧气是否已满 |
| D、集气瓶口向下收集氧气,收集完毕正放在桌面上 |
化学概念在逻辑上存在如图所示关系,对下列概念间的关系,说法正确的是( )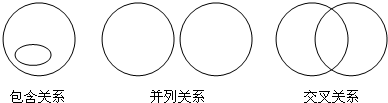

| A、纯净物与混合物属于包含关系 |
| B、化学反应与化合反应属于包含关系 |
| C、化合反应与分解反应属于交叉关系 |
| D、氧化反应与化合反应属于并列关系 |
下列关于空气成分用途的说法不正确的是( )
| A、用氧气急救病人 |
| B、将氧气和氮气混合充入灯泡,使灯炮耐用 |
| C、用氧气进行气焊 |
| D、食品充入氮气可延长保质期 |