题目内容
19.如图是钠与氯气(Cl2)反应生成氯化钠的模拟图.从图示可知下列说法不正确的是( )
| A. | 反应中钠原子转移一个电子给氯原子 | |
| B. | 钠离子与钠原子有相似的化学性质 | |
| C. | 核外电子在化学反应中起着重要作用 | |
| D. | 氯化钠由氯离子和钠离子构成 |
分析 根据图中所示.钠原子在化学反应中失去电子变为稳定结构,氯原子得到电子变为稳定结构,形成化合物氯化钠.
解答 解:A、由图可知钠原子失去电子,而氯原子得到电子,即反应中钠原子转移一个电子给氯原子,故正确;
B、钠离子与钠原子失去1个电子形成的离子,故两者的化学性质一定不同;故错误;
C、原子是因为核外电子的得失使其变为稳定结构,所以核外电子在化学反应中起着重要作用,故正确;
D、氯化钠由氯离子和钠离子构成,故正确.
故选B.
点评 学生应正确分析图中提供的信息和教材所学知识的密切联系,认识电子在化学反应中的重要作用.

练习册系列答案
相关题目
9.某原子的第一电子层有2个电子,第二电子层有6个电子,它属于( )
| A. | 非金属元素 | B. | 金属元素 | C. | 稀有气体元素 | D. | 无法判断 |
14.下列哪位科学家提出了元素周期律并画出了第一张元素周期表( )
| A. | 道尔顿 | B. | 普利斯特里 | C. | 门捷列夫 | D. | 阿伏加德罗 |
8.连接下列连接仪器中不能够用水润湿的是( )
| A. |  连接玻璃管与带孔橡胶塞 | B. |  连接玻璃管与胶皮管 | ||
| C. |  连接试管与橡胶塞 | D. |  连接长颈漏斗与带孔橡胶塞 |
9.“数字化实验”丰富了实验研究的方法,它可将实验过程中某些因素(酸碱性、气压等)的变化以数据、图象的形式呈现出来.请回答:
Ⅰ.探究二氧化碳与水的反应
①图1中可观察到甲试管中的紫色液体变为红色,写出发生反应的化学方程式CO2+H2O→H2CO3,乙试管的作用是对照;
②由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变强(填“强”或“弱”).
Ⅱ.探究蜡烛燃烧的产物
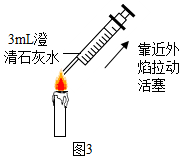
③如图3所示,用注射器在蜡烛外焰部位抽气并振荡,可观察到石灰水变浑浊,证明反应生成了二氧化碳;若将干冷的烧杯罩在火焰上方,观察到烧杯内壁有水雾,证明反应生成了水.
④如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线b、c(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水.
Ⅱ.比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
⑤写出碳酸钙与稀盐酸发生反应的化学方程式CaCO3+2HCl→CaCl2+H2O+CO2↑;
图5中,乙试管中稀盐酸的浓度C%应为10%;
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是反应物之间的接触面积更大.
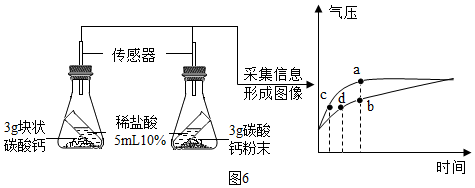
⑥按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示.对比分析坐标图中的点c、d(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短.
Ⅰ.探究二氧化碳与水的反应
| 方案一 | 方案二(数字化实验) |
 | 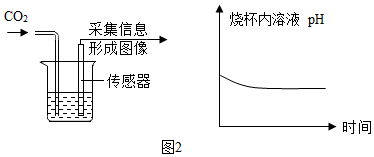 |
②由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变强(填“强”或“弱”).
Ⅱ.探究蜡烛燃烧的产物
| 方案一 | 方案二(数字化实验) |
 |  |
④如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线b、c(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水.
Ⅱ.比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
⑤写出碳酸钙与稀盐酸发生反应的化学方程式CaCO3+2HCl→CaCl2+H2O+CO2↑;
| 方案一 | 方案二(数字化实验) |
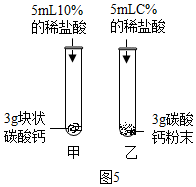 |  |
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是反应物之间的接触面积更大.
⑥按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示.对比分析坐标图中的点c、d(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短.
 根据如图结构示意图,用化学符号表示下列微粒
根据如图结构示意图,用化学符号表示下列微粒