题目内容
(2013?重庆)葡萄糖(C6H12O6)是人体重要的供能物质,每克葡萄糖完全代谢释放的能量为16kJ(表示为16kJ/g).葡萄糖在体内代谢的化学方程式为:C6H12O6+6O2
6CO2+6H2O.某病人需要输入5%的葡萄糖注射液500mL(密度近似为1g/cm3).计算:
(1)配制上述注射液所需20%的葡萄糖溶液的质量、蒸馏水的质量.
(2)若上述注射液中的葡萄糖完全代谢,理论上消耗氧气的质量是多少?释放出的能量是多少?
| 酶 |
(1)配制上述注射液所需20%的葡萄糖溶液的质量、蒸馏水的质量.
(2)若上述注射液中的葡萄糖完全代谢,理论上消耗氧气的质量是多少?释放出的能量是多少?
分析:溶液稀释前后,溶质的质量不变;
根据化学方程式可以进行相关方面的计算.
根据化学方程式可以进行相关方面的计算.
解答:解:(1)解:设所需20%的葡萄糖溶液的质量为X,
500mL葡萄糖注射液的质量为:1g/cm3×500mL=500g,
根据稀释前后,溶质葡萄糖的质量不变,所以有:
X×20%=500g×5%
X=125g,
则所需要的蒸馏水的质量为:500g-125g=375g,
答:配制上述注射液所需20%的葡萄糖溶液的质量、蒸馏水的质量分别为125g、375g.
(2)解:设理论上消耗氧气的质量为Y,
5%的葡萄糖注射液500mL中,含有葡萄糖的质量为:500g×5%=25g,
C6H12O6+6O2
6CO2+6H2O
180 192
25g Y
=
Y≈26.7g,
释放出的能量是:16kJ/g×25g=400kJ,
答:上述注射液中的葡萄糖完全代谢,理论上消耗氧气的质量是26.7g,释放出的能量是400kJ.
500mL葡萄糖注射液的质量为:1g/cm3×500mL=500g,
根据稀释前后,溶质葡萄糖的质量不变,所以有:
X×20%=500g×5%
X=125g,
则所需要的蒸馏水的质量为:500g-125g=375g,
答:配制上述注射液所需20%的葡萄糖溶液的质量、蒸馏水的质量分别为125g、375g.
(2)解:设理论上消耗氧气的质量为Y,
5%的葡萄糖注射液500mL中,含有葡萄糖的质量为:500g×5%=25g,
C6H12O6+6O2
| 酶 |
180 192
25g Y
| 180 |
| 192 |
| 25g |
| Y |
Y≈26.7g,
释放出的能量是:16kJ/g×25g=400kJ,
答:上述注射液中的葡萄糖完全代谢,理论上消耗氧气的质量是26.7g,释放出的能量是400kJ.
点评:本题考查了溶液的稀释、根据化学方程式计算等方面的知识,要认真计算,以免疏漏.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目

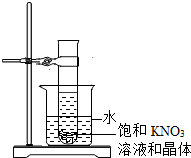 (2013?重庆模拟)某温度下,向盛有几小粒KNO3晶体的试管中,加入10g、10% KNO3的饱和溶液甲,并固定在盛有水的烧杯中(如图所示).向烧杯中加入某种物质后并搅拌,试管中的晶体消失了,得到KNO3 的溶液乙.
(2013?重庆模拟)某温度下,向盛有几小粒KNO3晶体的试管中,加入10g、10% KNO3的饱和溶液甲,并固定在盛有水的烧杯中(如图所示).向烧杯中加入某种物质后并搅拌,试管中的晶体消失了,得到KNO3 的溶液乙.