题目内容
2、二氧化碳气体
能
溶于水,在通常情况下,1 L水中约能溶解1L
二氧化碳气体.二氧化碳能与水反应生成碳酸
,反应式为二氧化碳+水→碳酸
.分析:本题主要考查二氧化碳的物理性质(水溶性)与化学性质(能与水反应);题目简单,根据课本内容填写即可.
解答:解:气体的水溶性一般可分为极易溶于水、易溶于水、能溶于水、不易溶于水、难溶于水几种情况.
二氧化碳属于能溶于水而不是易溶于水,溶于水后很少一部分二氧化碳与水反应生成碳酸.
故答案为:能,1L,碳酸,二氧化碳+水→碳酸.
二氧化碳属于能溶于水而不是易溶于水,溶于水后很少一部分二氧化碳与水反应生成碳酸.
故答案为:能,1L,碳酸,二氧化碳+水→碳酸.
点评:二氧化碳溶于水和与水反应不能混为一谈,能溶于水为物理性质,与水反应属于化学性质;1 L水中约能溶解 1L二氧化碳气体,而这1L气体中绝大部分一二氧化碳分子的形式存在于水中,只有1%左右的二氧化碳与水反应生成了碳酸.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
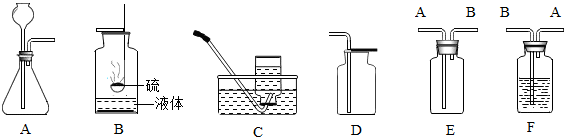 A来制取氧气,写出该反应的化学方程式
A来制取氧气,写出该反应的化学方程式 实验室常用稀盐酸和石灰石反应制取二氧化碳.
实验室常用稀盐酸和石灰石反应制取二氧化碳.
