题目内容
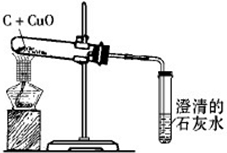 如图是用木炭粉还原氧化铜的实验装置图,请按要求回答:
如图是用木炭粉还原氧化铜的实验装置图,请按要求回答:(1)实验过程中你看到的实验现象有哪些?
(2)大试管中发生的反应方程式为:
(3)反应完成后,实验操作应先
(4)实验时,酒精灯加铁丝网罩的目的是
(5)在上述化学反应中,被还原的物质是
(2)根据大试管中发生的反应,写出的反应方程式;
(3)根据停止加热时试管内压强减小分析实验的操作;
(4)根据木炭还原氧化铜的条件分析;
(5)根据在上述化学反应中得失氧的物质进行分析.
(2)由上述分析可知,大试管中发生的反应方程式为:C+2CuO
| ||
(3)反应完成后,为了防止停止加热时试管内压强减小,石灰水倒流到热的试管引起试管的炸裂.所以,实验操作是:应先将导管从石灰水中移出,后熄灭酒精灯.
(4)木炭还原氧化铜的条件是高温,酒精灯加网罩的目的是:集中火焰提高温度;
(5)在上述反应中,氧化铜中的氧失去了生成了铜,被还原;碳夺取了氧化铜中的氧生成了二氧化碳被氧化.这个反应说明碳可以用来作还原剂.
故答为:(1)黑色粉末变红色;澄清的石灰水变浑浊.(2)C+2CuO
| ||

 名校课堂系列答案
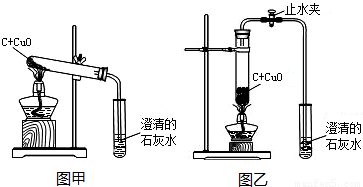
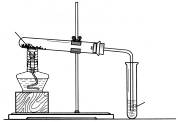
名校课堂系列答案梧州市某中学化学兴趣小组按照课本实验方法(如图19甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。
 |
| ||||
| ||||
|
|
|
【提出问题】暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为 。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是 。
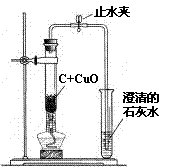
(2)小周建议用图19的乙装置替代甲装置。与甲相比较,乙装置中将试管直立放
置的作用是 。
(3)对下列三种氧化铜和碳的质量比例,小施建议选择 (填选项序号)的比例。
A. 32︰3 B. 40︰3 C. 48︰3
你认为小施这样选择的理由是 。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙装置的 后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时, (填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是 (填“吸”或“放”)热反应。
待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是 。
待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
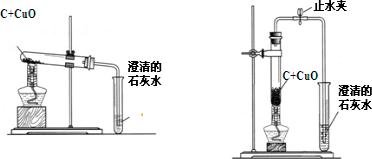

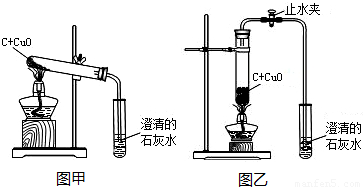 梧州市某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.
梧州市某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.