题目内容
9.关于液氧与氧气的下列说法,正确的是( )| A. | 两者属于不同的物质 | B. | 两者的构成微粒不同 | ||
| C. | 两者的化学性质不同 | D. | 构成两者的微粒间的距离不同 |
分析 液氧与氧气属同种物质的不同状态,结构相同都是有氧气分子构成的,而分子是保持物质化学性质的微粒.
解答 解:
A、液氧与氧气状态不同,属于同一种物质,故错误;
B、液氧与氧气状态不同,但构成的分子相同,都是由氧气分子构成的,故错误;
C、由分子的定义可知,两者的化学性质应该相同,而物理性质不同,故错误;
D、液氧和氧气的化学性质相同,但物理性质不同,其状态、微粒间的距离不同,故正确.
答案:D.
点评 此题是对氧气有关问题的考查,解题的关键是对液氧及氧气构成的认识,属基础性知识考查题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列各组物质中,前者属于化合物、后者属于混合物的是( )
| A. | 碘酒、二氧化碳 | B. | 冰水共存物、食盐 | ||
| C. | 红磷、纯碱 | D. | 净化后的空气、大理石 |
4.水是生产生活中不可缺少的物质.下列关于水的说法中正确的是( )
| A. | 明矾溶液可以区分硬水和软水 | |
| B. | 水与过氧化氢的组成元素相同,均可用于制备氧气 | |
| C. | 在自来水厂净化水的过程中,发生的变化都是物理变化 | |
| D. | 为了节约用水,可以用工业废水直接浇灌农田 |
1.能将氯化钠、氯化镁和氯化银固体混合物逐一分离,可选用的一组试剂是( )
| A. | 水、硝酸银、稀盐酸 | B. | 水、氢氧化钠溶液、盐酸 | ||
| C. | 水、氢氧化钾溶液 | D. | 水、碳酸钾溶液、稀硫酸 |
19.对空气中氧气含量测定的再认识.
Ⅰ.用燃烧法测定空气中氧气含量
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的文字表达式红磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶中.用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【实验过程】
甲小组同学使用图1装置进行实验,实验前应先进行的操作是检查装置气密性;

(1)用止水夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞;
(3)燃烧结束,充分冷却,打开止水夹;
(4)观察并记录水面的变化情况.
【问题提出】该小组同学多次实验发现,集气瓶内上升的水面始终小于理论值.经查阅资料知:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
Ⅱ.改进空气中氧气含量测定的方法
【实验改进】经查阅资料可知:常温下,铁在潮湿的空气中会生锈,因为铁与空气中的氧气、少量水反应生成铁锈(其主要成分是Fe2O3),但速度缓慢.在有食盐(NaCl)、活性炭存在条件下,反应速度较快.乙小组选择该原理,设计了如图2所示实验装置图.
【数据处理】乙小组同学用量筒测量实验前后烧杯中水的体积,测得实验数据如下表:
根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.4%(计算结果精确到0.1%).
【实验反思】与燃烧红磷方法相比,乙小组方法测定空气中氧气含量的优点是充分消耗氧气,测定的结果更准确.
实验再改进】在乙组实验的基础上,丙组同学设计了如图3的装置进行氧气含量的测定,其方法如下:
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(即食盐水、铁粉、活性炭的混合物,体积为2mL),封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至注射器示数不再发生变化时停止实验.
【实验再反思】
丙小组同学的方案与乙小组的方案同学相比,优点是能够较为准确观察示数变化,实验更直观.
Ⅰ.用燃烧法测定空气中氧气含量
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的文字表达式红磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶中.用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【实验过程】
甲小组同学使用图1装置进行实验,实验前应先进行的操作是检查装置气密性;

(1)用止水夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞;
(3)燃烧结束,充分冷却,打开止水夹;
(4)观察并记录水面的变化情况.
【问题提出】该小组同学多次实验发现,集气瓶内上升的水面始终小于理论值.经查阅资料知:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
Ⅱ.改进空气中氧气含量测定的方法
【实验改进】经查阅资料可知:常温下,铁在潮湿的空气中会生锈,因为铁与空气中的氧气、少量水反应生成铁锈(其主要成分是Fe2O3),但速度缓慢.在有食盐(NaCl)、活性炭存在条件下,反应速度较快.乙小组选择该原理,设计了如图2所示实验装置图.
【数据处理】乙小组同学用量筒测量实验前后烧杯中水的体积,测得实验数据如下表:
| 测量 项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的体积 | |
| 体积/mL | 60.0 | 34.5 | 125.0 |
【实验反思】与燃烧红磷方法相比,乙小组方法测定空气中氧气含量的优点是充分消耗氧气,测定的结果更准确.
实验再改进】在乙组实验的基础上,丙组同学设计了如图3的装置进行氧气含量的测定,其方法如下:
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(即食盐水、铁粉、活性炭的混合物,体积为2mL),封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至注射器示数不再发生变化时停止实验.
【实验再反思】
丙小组同学的方案与乙小组的方案同学相比,优点是能够较为准确观察示数变化,实验更直观.
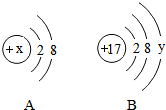 化学用语是最简明、信息丰富、国际通用的语言.
化学用语是最简明、信息丰富、国际通用的语言.