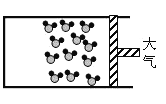
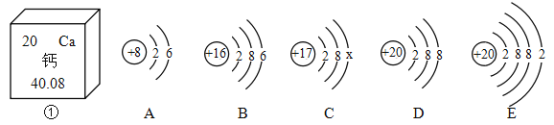
题目内容
过氧化氢(H2O2)广泛应用于纺织、医药、卫生行业,常作漂白剂和消毒剂。
(1)过氧化氢与_________(填物质名称)组成元素相同。
(2)过氧化氢中氧元素的化合价是______________。
(3)向盛有硫酸和高锰酸钾稀溶液的试管中加入足量过氧化氢溶液,发生下列反应: 5H2O2+2KMnO4+3H2SO4=K2SO4+2MnSO4+8H2O+5_______↑。
为检验生成的气体,应进行的操作是__________。
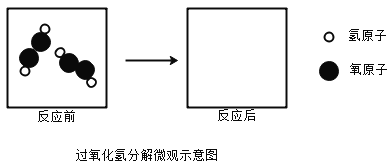
(4)请将下图反应后的物质微观示意图补充完整,要求能体现质量守恒定律。_________
某化学兴趣小组对“大理石与稀盐酸反应快慢的影响因素”进行了探究。
(提出问题)大理石与稀盐酸反应的快慢受哪些因素的影响呢?
(猜想与假设)A.可能与稀盐酸的质量分数有关;B.可能与大理石形状有关。
(设计并实验)用不同质量分数的稀盐酸和不同形状的大理石进行如下实验:
实验编号 | 稀盐酸的质量分数(均取20ml) | 大理石的形状(均取3g) | 二氧化碳的体积/ml(均收集1分钟) |
① | 5% | 块状 | 28.3 |
② | 5% | 粉末 | 46.8 |
③ | 10% | 块状 | 58.7 |
④ | 10% | 粉末 | 丢失 |
(收集证据)要比较不同形状的大理石对反应快慢的影响,应选择的实验编号是___________。
(得出结论)完成①③两组实验后得出的结论是:______________。
(评价与反思)下表是第①组实验的详细数据。
时段/秒 | 0~30 | 30~60 | 60~90 | 90~120 | 120~150 | 150~180 |
CO2的体积/ mL | 8.1 | 20.2 | 11.9 | 9.6 | 7.6 | 6.1 |
(1)上述表格可知,从第60秒开始反应的速率减慢,其原因是____。
(2)由于没有及时记录数据,导致第④组实验数据丢失,你认为合理的数据是_______(填序号)。
A 45.7 B 54.7 C 95.4
下列物质的性质与用途不对应的是 ( )
选项 | 物质的性质 | 物质的用途 |
A | 碳具有还原性 | 可用于炼铁 |
B | 铜有导电性 | 可做电线 |
C | 氮气的化学性质不活泼 | 可用作保护气 |
D | 铝具有良好的导热性 | 可用铝制作耐腐蚀的窗框 |
A.A B.B C.C D.D
下面是小婷同学测定黄铜(铜锌合金)中铜的质量分数的过程。小婷同学取10 g黄铜于烧杯中,将120 g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 29.96 | 49.92 | m | 89.84 | 109.8 | 129.8 |
①10g黄铜完全反应产生H2的质量________g;
②表中m=________;
③求黄铜中铜的质量分数________ (写出计算过程)。
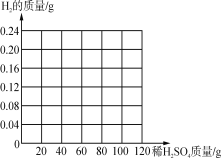
④请在如图画出10g黄铜加入稀硫酸与生成氢气的质量的图象________。


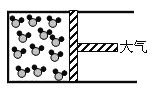
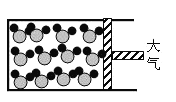 B.
B.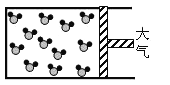 C.
C.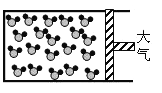 D.
D.