题目内容
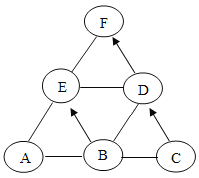
【题目】现有一包固体混合物A,可能是氯化铵、碳酸钠、碳粉和氧化铜中的一种或几种,为检验其组成,某同学设计了如下流程(假设过程中所有发生的反应均恰好完全反应):
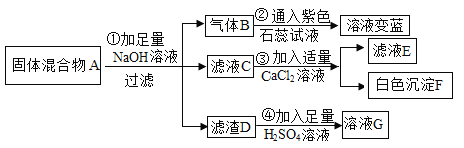
(1)气体B是具有________________________气味的气体。
(2)白色沉淀F的化学式为_______________________________。
(3)步骤④中发生反应的化学方程式为_______________________________。
(4)通过上述现象分析判断,固体混合物A中一定含有的物质是_______________________________,一定不含的物质是_______________________________。
【答案】刺激性 CaCO3 ![]() 氯化铵 、碳酸钠、氧化铜 碳粉
氯化铵 、碳酸钠、氧化铜 碳粉
【解析】
由流程图可知混合物A可能是氯化铵、碳酸钠、碳粉和氧化铜中的一种或几种,与适量氢氧化钠溶液反应后生成能使紫色石蕊溶液变蓝的气体,说明该气体为氨气,氨气具有刺激性气味,则混合物中一定含有氯化铵;滤液C中加人适量氯化钙溶液,有沉淀生成,说明混合物中含有碳酸钠,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠;滤渣D中加入稀硫酸,得到溶液G,说明滤渣全部溶解,则滤渣D中只含有CuO,不含碳粉。
(1)气体B为氨气,氨气具有刺激性气味。
(2)向滤液C中加入适量氯化钙溶液,有沉淀生成,说明混合物中含有碳酸钠,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,因此白色沉淀F的化学式为CaCO3。
(3)步骤④滤渣D中加入稀硫酸得到溶液G,说明滤渣全部溶解,则滤渣D中只含有CuO,氧化铜和硫酸反应生成硫酸铜和水,反应的化学方程式为![]() 。
。
(4)综上所述混合物A中一定有氯化铵、碳酸钠、氧化铜,滤渣D经过反应④全部溶解,说明混合物中一定不含碳粉。