题目内容
8.元素周期表是学习和研究化学的重要工具,请分析图中的信息回答有关问题:
(1)3号元素形成的离子符号是Li+.
(2)8号元素和16号元素化学性质相似的原因是它们的原子最外层电子数相同.
(3)写出12号与9号元素组成化合物的化学式MgF2.
(4)请结合图1、图2,推断碘元素在周期表中位于第五周期.
分析 (1)根据第3号元素的名称是锂元素以及锂元素的原子,最外层电子数为1,易失去1个电子形成的阳离子进行解答;
(2)根据原子的最外层电子数相同,化学性质相似解答;
(3)根据化学式的写法进行解答;
(4)根据电子层数决定周期数解答.
解答 解:(1)根据元素周期表中所提供的信息可查得:第3号元素的名称是锂元素,锂元素的原子,最外层电子数为1,易失去1个电子形成的阳离子,符号为:Li+;
(2)8号元素和16号元素的最外层电子数都是6,化学性质相似的原因是它们的原子最外层电子数相同;
(3)12号元素和9号元素分别是Mg和F,镁元素的原子,最外层电子数为2,易失去2个电子形成的阳离子,F元素的原子,最外层电子数为7,易得到1个电子形成的阴离子,形成化合物的化学式为MgF2;
(4)根据元素周期律电子层数等于周期数,碘元素的原子核外有5个电子层,在周期表中位于第五周期.
答案:
(1)Li+;
(2)最外层电子数;
(3)MgF2;
(4)五.
点评 本题考查学生对元素周期表中的一些变化规律的归纳和总结,并学以致用.明确原子与离子的结构示意图的特点,并会根据原子结构示意图判断元素的化合价,会根据化合价书写化学式.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
18. 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
 向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )
向一定质量的Na2CO3,Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法符合反应事实的是( )| A. | 在0-a段发生3个化学反应 | |
| B. | c点的沉淀是BaSO4 | |
| C. | 图中m点的值是2.33 | |
| D. | 取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量 |
19.下列区分各组物质的两种方案都合理的是( )
| 选项 | A | B | C | D |
| 物质 | 碳酸钠和氢氧化钠 | 空气和氧气 | 尿素和硫酸铵 | 木炭和二氧化锰 |
| 方案一 | 稀盐酸 | 带火星的木条 | 氢氧化钠溶液 | 观察颜色 |
| 方案二 | 酚酞试液 | 燃烧的木条 | 加水 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
16.物质 A 和 B 点燃条件下反应生成 C 和 D,反应前后分子变化的微观示意图如下:
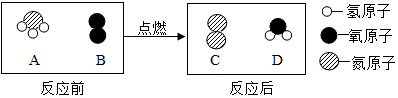
(注意:图示中没有表示物质间的微粒数量关系)
下列说法不正确的是( )

(注意:图示中没有表示物质间的微粒数量关系)
下列说法不正确的是( )
| A. | 该反应中 B 为氧化剂 | |
| B. | 生成的 C和D 的化学计量数之比为 1:1 | |
| C. | 该反应属于置换反应 | |
| D. | 该反应肯定有元素的化合价发生改变 |
20.推理是化学学习中常用的思维方法,以下推理中正确的是( )
| A. | 酸与碱发生中和反应时生成盐和水,因此有盐和水生成的反应一定是中和反应 | |
| B. | 碱性溶液能使石蕊试液变蓝,能使石蕊试液变蓝的溶液一定呈碱性 | |
| C. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| D. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 |