题目内容
9. 如表是元素周期表中部分元素的原子结构示意图,请分析:
如表是元素周期表中部分元素的原子结构示意图,请分析:(1)在化学反应中Mg原子易失(填“得”或“失”)电子;
(2)Na+离子核外的电子数为10,Ca原子中的x=8;
(3)经分析发现,元素的周期数与原子的电子层数、元素的主族数与原子的最外层电子数有着密切的关系;请推断M原子的最外层电子数为3,N原子的电子层数为4;
(4)若镓(Ga)元素与氯元素只组成一种化合物,请写出该化合物的化学式GaCl3.
分析 (1)根据原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子;进行解答.
(2)根据镁原子的结构示意图分析,根据核内质子数等于核外电子数;
(3)根据元素周期表的信息来分析;
(4)根据镓元素最外层电子数分析化合价,根据化合价书写化学式.
解答 解:(1)根据金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子,可知钠原子在化学反应中易失电子,形成阳离子;故填:失;
(2)由镁原子的结构示意图可知,最外层有2个电子,易失去变成镁离子,(Mg2+)核外有10个电子,核内质子数等于核外电子数,Ca原子中的x=8,故填:10;8;
(3)根据根据元素周期律:同一纵行,原子最外层电子数相同;可推断M原子的最外层电子数为3,根据根据元素周期律:电子层数等于周期数;可推断N原子的电子层数为4.故填:3;4;
(4)由原子结构示意图可知镓(Ga)元素原子最外层上有3个电子,易失去三个电子达到稳定结构,镓元素在形成化合物时显+3价,氯元素显-1价,化合价交叉得化学式为GaCl3.故填:GaCl3.
故答案为:(1)失;(2)10;8;(3)3;4;(4)GaCl3.
点评 本题考查学生对原子结构示意图、元素周期律知识的理解与在解题中灵活应用的能力.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
19.下列实验操作中正确的是( )
| A. |  | B. |  | C. |  | D. |  |
4.下列属于化学变化的是( )
| A. | 冰雪融化 | B. | 铁器生锈 | C. | 汽油挥发 | D. | 西瓜榨汁 |
1.下列关于微观粒子的说法中,错误的是( )
| A. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| B. | “墙内开花墙外香”--分子在不断的运动 | |
| C. | 水烧开后易把壶盖冲起--温度升高,分子变大 | |
| D. | 在化学变化中,分子可以再分,原子不可再分 |
18.如图为元素周期表的一部分(X元素信息不全).下列说法正确的是( )
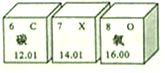

| A. | 氧的化学性质不活泼 | B. | X表示N2 | ||
| C. | 碳原子的质子数是6 | D. | 三种元素原子的核外电子数相同 |

 请仔细观察如图,指出倾倒液体操作中的错误之处:
请仔细观察如图,指出倾倒液体操作中的错误之处: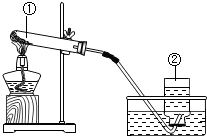 成了浅紫红色,你认为产生该现象的原因可能是试管口未塞一团棉花.
成了浅紫红色,你认为产生该现象的原因可能是试管口未塞一团棉花.