题目内容
13.化学实验中常用的装置如下,请回答下列问题.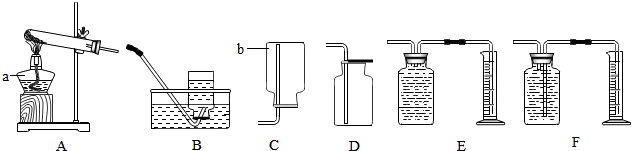
①写出仪器a和b的名称:a酒精灯,b集气瓶.
②实验室制取氧气时可以选择的收集装置是D或F(填仪器编号).用氯酸钾和二氧化锰为原料制取氧气,催化剂是二氧化锰.
③连接A、F(E/F)装置,点燃酒精灯,收集氧气并测定其体积.该方法收集到的氧气往往不纯,这对氧气体积的测定没有(填“有”或“没有”)影响,不纯的原因是试管中的空气进入集气瓶中.
④A中有氯酸钾0.02mol,若完全分解可生成多少摩尔氧气?0.03mol(写出计算过程).
⑤经测定反应生成了0.32g氧气,这些氧气的物质的量是0.01mol.
此时,A中的氯酸钾没有(填“有”或“没有”)完全分解.
分析 ①熟记常见仪器的名称;
②根据氧气的性质来分析其收集方法,为了加快氯酸钾的分解可加入二氧化锰来做催化剂;
③试管内开始有空气,产生气泡后立即收集,会导致收集到的气体中含有空气而不纯,但对于气体体积测定没有影响,因为试管内开始有空气最后是氧气,进入集气瓶中的气体体积不变;
④根据方程式列比例式进行计算;
⑤根据质量与物质量的关系考虑本题.
解答 解:①a是酒精灯,b是集气瓶;故填:酒精灯;集气瓶;
②因为氧气的密度比空气大,且不易溶于水,故可用排水法或向上排空气法来收集;二氧化锰能加快氯酸钾的反应速率,且其质量和化学性质在反应前后没有发生改变,所以在该反应中充当催化剂;故填:D或F;二氧化锰;
③连接AF,产生气泡后立即收集氧气并测定其体积,对氧气体积的测定没有影响,不纯的原因是试管中的空气进入集气瓶中.故填:F;没有;试管中的空气进入集气瓶中;
④设完全分解可生成氧气的物质量为X:
2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑
2 3
0.02mol X
$\frac{2}{3}=\frac{0.02mol}{X}$
X=0.03mol;故填:0.03;
⑤氧气的物质的量为:$\frac{0.32g}{32g/mol}$=0.01mol,由于根据第④步可知氯酸钾完全分解得到氧气0.03mol,所以生成0.01mol氧气说明氯酸钾没有完全反应.
故填:0.01;没有.
点评 通过回答本题知道了氧气的收集方法和气体体积的测定方法,物质的质量、物质量、摩尔质量的关系.

练习册系列答案
相关题目
3.涛涛同学梳理了以下知识:①用酒精浸泡捣烂的某些植物的花瓣可制得酸碱指示剂;②用水灭火降低了可燃物的着火点;③生活中使用的洗发液一般是弱碱性的;④自制简易净水器中的活性炭可降低水的硬度;⑤厨房天然气管道漏气,应立即打开排风扇通风;⑥加熟石灰研磨可鉴别氯化铵和硫酸钾;⑦有盐和水生成的反应一定是中和反应.其中正确的是( )
| A. | ①③⑥ | B. | ②③⑦ | C. | ①⑤⑥⑦ | D. | ②④⑤ |
4.填表:
| 化学符号 | O2 | 2He | $\stackrel{+2}{Ca}$ | ||
| 表示意义 | 钠元素 | 1个锌原子 |
1.填写化学方程式并简答有关的内容:
| 化学反应 | 化学方程式 | 简答 |
| 铁丝在纯氧中燃烧 | 生成物的颜色为黑色 | |
| 红磷燃烧 | 反应物的物质的量之比为4:5. | |
| 硫酸铜溶液中加入氢氧化钠溶液 | 现象:产生蓝色沉淀 | |
| 硫在氧气中燃烧 | 生成物会引起的一种环境问题是形成酸雨 |
8.下列实验操作正确的是( )
| A. |  | B. |  | C. |  液体加热 | D. |  |
 鉴定是常用的物质检验方法之一,是根据一种物质的特殊性质,用化学方法检验它是不是这种物质.
鉴定是常用的物质检验方法之一,是根据一种物质的特殊性质,用化学方法检验它是不是这种物质.