题目内容
某磁铁矿(主要成分为Fe3O4)500t,经测得含铁217.3t,求该铁矿石含Fe3O4的质量分数.
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:根据题意,某磁铁矿(主要成分为Fe3O4)500t,经测得含铁217.3t,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:某磁铁矿(主要成分为Fe3O4)500t,经测得含铁217.3t,该铁矿石含Fe3O4的质量为217.3t÷(
×100%)≈374.7t.
该铁矿石含Fe3O4的质量分数为
×100%≈74.9%.
答:该铁矿石含Fe3O4的质量分数为74.9%.
| 56×3 |
| 56×3+16×4 |
该铁矿石含Fe3O4的质量分数为
| 374.7t |
| 500t |
答:该铁矿石含Fe3O4的质量分数为74.9%.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
钛是21世纪重要金属,许多领域中将代替钢铁,钛酸亚铁(FeTiO3)可以用来冶炼金属钛,其中钛元素的化合价是( )
| A、-4 | B、-2 | C、+4 | D、+2 |
已知锌、镁与稀硫酸反应的化学方程式为:Mg+H2SO4=MgSO4+H2↑,Zn+H2SO4=ZnSO4+H2↑.相同质量的锌和镁分别于镁分别和足量的稀硫酸反应,产生的氢气的质量比是( )
| A、65:24 | B、24:65 |
| C、1:1 | D、无法确定 |
如图,过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气.下列现象正确的是( )
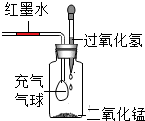

| A、气球胀大,红墨水左移 |
| B、气球缩小,红墨水左移 |
| C、气球胀大,红墨水右移 |
| D、气球缩小,红墨水右移 |
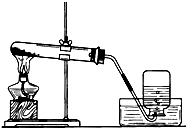
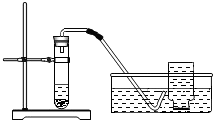
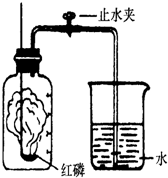 某同学设计了测定空气中氧气含量的实验,实验装置如图.
某同学设计了测定空气中氧气含量的实验,实验装置如图.