题目内容
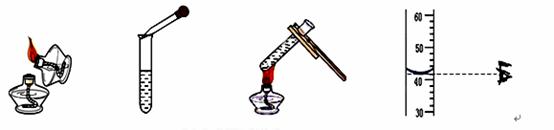
某同学设计如图所示的实验装置,进行一氧化碳还原氧化铁的实验.试回答:
(1)该装置存在的一个主要问题是 ,你的改进方法是 .
(2)实验过程中图A处玻璃管中能观察到的实验现象是 ,发生反应的化学方程式为 .
(3)B处观察到的实验现象是 .该同学实验完成后,发现过量的澄清石灰水增重0.44g,则通入装置的CO气体质量 (填“>”、“<”或“=”)0.28g.

| 一氧化碳还原氧化铁;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 金属与金属材料. |
| 分析: | (1)根据一氧化碳的毒性和可燃性分析回答; (2)根据一氧化碳与氧化铁的反应,分析现象、写出方程式; (3)根据二氧化碳与氢氧化钙的反应分析B处观察到的实验现象,根据实验的注意事项分析通入一氧化碳的质量. |
| 解答: | 解:(1)由于一氧化碳是有毒、具有可燃性的气体,所以,该装置存在的一个主要问题是:尾气没有进行处理,会污染空气,你的改进方法是:点燃或收集. (2)由于在高温条件下一氧化碳将氧化铁还原成铁,生成了二氧化碳.所以,实验过程中图A处玻璃管中能观察到的实验现象是:红色粉末变成黑色,发生反应的化学方程式为:3CO+Fe2O3 (3)由于一氧化碳与氧化铁反应生成二氧化碳能与氢氧化钙反应,所以B处观察到的实验现象是:澄清石灰水变浑浊.该同学实验完成后,发现过量的澄清石灰水增重0.44g,由方程可知,参见反应的一氧化碳的质量是2.8g,由于实验前通入一氧化碳,反应后还要继续通入一氧化碳,所以,通入装置的CO气体质量>0.28g. 故答为:(1)尾气没有进行处理,会污染空气 点燃或收集;(2)红色粉末变成黑色 3CO+Fe2O3 |
| 点评: | 本题主要考查了一氧化碳与氧化铁反应的现象、一氧化碳的性质、对大气的污染等知识,难度不大,属于基础性的练习题. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案用CO还原铁的氧化物1.00g,得到铁粉0.75g,则下列说法中正确的是( )
|
| A. | 该氧化物是Fe2O3 |
|
| B. | 该氧化物可能是由FeO、Fe2O3、Fe3O4组成的混合物 |
|
| C. | 该氧化物是FeO |
|
| D. | 该氧化物中不含FeO |
 2Fe+3CO2.
2Fe+3CO2.
 ,( );
,( );
 下列说法不正确的是
下列说法不正确的是  学反应。请与他们一起完成实
学反应。请与他们一起完成实