题目内容
电解水时,为了增强溶液的导电性.常常在水中加入稀H2SO4或氢氧化钠溶液以加快电解速度.现有溶质质量分数为8%的稀H2SO4溶液25 g,通电电解一段时间后,稀H2SO4的溶质质量分数增加到10%,求这段时间内电解水所产生的氧气质量为多少(g)?
答案:
电解前:m(稀硫酸) =8%*25=2g m(水)=23g 电解后:m(稀硫酸) =2g ,2/10%=20g,说明m(溶液)=20g 所以m(水)=20-2=18 所以,水减少5g 电离方程式: 2 H2O = 2 H2 +O2 36 32 5 X X=4.44g

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目

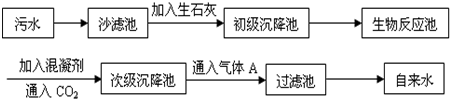
 3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:
3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题: