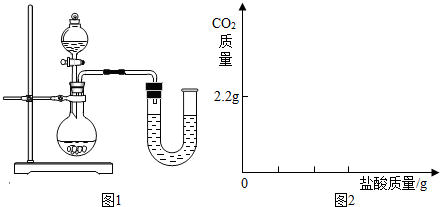
题目内容
(1) 2.2g
(2) 解:设纯碱试样中碳酸的质量为x。
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑ (1分)
106 44
x 2.2g (1分)
![]() (1分)
(1分)
x=5.3g (1分)
试样中碳酸钠的质量分数为:
![]() (1分)
(1分)
答:略。
(3)NaCl、HCl
某学习小组同学用右图试剂中的过氧化钠溶液制取氧气,取该溶液17g,加入适量MnO2充分反应。完成下列分析及计算:
⑴小明根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为:生成氧气的质量=17g×5%×![]() ×100%=17g×5%×
×100%=17g×5%×![]() ×100%。
×100%。
老师指出小明的计算是错误的,你认为错误的原因是
(填字母序号)。
A.过氧化氢的相对分子质量计算有误
B.过氧化氢中的氧元素没有全部转移到氧气中
⑵请你根据化学方程式计算制取氧气的质量。

练习册系列答案
相关题目
某工厂生产的纯碱产品中含有少量杂质,为了验证该产品包装袋上碳酸钠≥96%的这个质量标志.某课外学习小组取11.0g该纯碱样品,用质量分数为10%的稀盐酸来进行测定(杂质不与稀盐酸反应),有关实验数据如下:
请据此回答以下问题:
(1)写出碳酸钠与稀盐酸反应的化学方程式 .
(2)测得11.0g该样品中所含的纯碳酸钠的质量为 g.由此证明该产品为
(填“合格”或“不合格”)产品.
(3)根据实验数据,在下图上绘制出所加稀盐酸质量与生成的气体质量关系的曲线.

| 所加稀盐酸的质量 | 18.25g | 36.5g | 54.75g | 73.0g | 100.0g |
| 产生的CO2的质量 | 1.1g | 2.2g | 3.3g | 4.4g | 4.4g |
(1)写出碳酸钠与稀盐酸反应的化学方程式
(2)测得11.0g该样品中所含的纯碳酸钠的质量为
(3)根据实验数据,在下图上绘制出所加稀盐酸质量与生成的气体质量关系的曲线.