题目内容
18.如图是实验室制取并探究二氧化碳性质的实验装置:
(1)仪器名称:E分液漏斗,它的优点是控制化学反应速率.
(2)锥形瓶A中的发生反应的文字表达式碳酸钙+盐酸→氯化钙+水+二氧化碳.
(3)广口瓶B中观察到的现象是澄清的石灰水变浑浊,其原理是二氧化碳+氢氧化钙→碳酸钙+水(用文字表达式表示).
(4)广口瓶C中观察到的现象是紫色的石蕊试液变红色,原因是二氧化碳+水→碳酸(用文字表达式表示).
(5)烧杯D中观察到的现象是下层蜡烛先灭,上层蜡烛后灭,因为二氧化碳不可燃,不助燃、密度比空气大.
分析 (1)熟记仪器的名称与用途;
(2)根据化学反应的原理以及文字表达式的写法来分析;
(3)根据二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水来分析;
(4)根据二氧化碳与水反应生成碳酸来分析;
(5)根据二氧化碳的密度比空气大,不燃烧也不支持燃烧来分析.
解答 解:(1)仪器E是分液漏斗,分液漏斗可以控制滴加液体试剂的速率来控制反应速率;故填:分液漏斗;控制化学反应速率;
(2)在实验室中,常用大理石或石灰石与稀盐酸反应来制取二氧化碳,同时生成氯化钙和水;故填:碳酸钙+盐酸→氯化钙+水+二氧化碳;
(3)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,所以观察到装置B中澄清的石灰水变浑浊,文字表达式为:二氧化碳+氢氧化钙→碳酸钙+水;故填:澄清的石灰水变浑浊;二氧化碳+氢氧化钙→碳酸钙+水;
(4)二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;故填:紫色的石蕊试液变红色;二氧化碳+水→碳酸;
(5)二氧化碳的密度比空气大,不燃烧、也不支持燃烧,所以烧杯D中观察到的现象是下层蜡烛先灭,上层蜡烛后灭;故填:下层蜡烛先灭,上层蜡烛后灭;二氧化碳不可燃,不助燃;密度比空气大.
点评 本题主要考查了二氧化碳的制取与收集方法、二氧化碳性质的探究,难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
14.甲、乙、丙三种物质的溶解度曲线如图所示.请你根据图判断,下列说法中不正确的是( )

| A. | 50℃时,甲物质的溶解度大于乙物质的溶解度 | |
| B. | 40℃时,甲、乙物质的饱和溶液中含有的溶质质量相等 | |
| C. | 甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲物质 | |
| D. | 30℃时,丙物质的饱和溶液溶质质量分数约为9.1% |
10.下列对NaOH和Ca(OH)2的性质叙述,错误的是( )
①都是白色固体 ②都易溶于水放出大量热③溶液都使酚酞试液变红 ④都能与酸发生反应 ⑤溶液通入CO2都变浑浊 ⑥与Na2CO3反应都变浑浊.
①都是白色固体 ②都易溶于水放出大量热③溶液都使酚酞试液变红 ④都能与酸发生反应 ⑤溶液通入CO2都变浑浊 ⑥与Na2CO3反应都变浑浊.
| A. | ② | B. | ⑤⑥ | C. | ①② | D. | ②⑤⑥ |
8.物质的名称、俗名、化学式完全一致的是( )
| A. | 碳酸钠 苏打 Na2CO3 | B. | 氯化氢 盐酸 HC1 | ||
| C. | 氧化钙 熟石灰 CaO | D. | 硫酸铜 胆矾 CuSO4 |

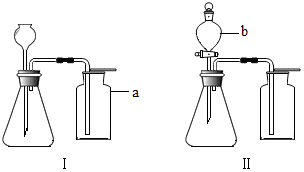 如图是气体制备的装置图.
如图是气体制备的装置图.
