题目内容
取某质量的下列四种物质,分别与稀盐酸充分反应,产生CO2最多的是( )
分析:我们可以先计算出要得到等质量的二氧化碳哪一种物质用的最少,则说明哪一种物质产生二氧化碳的能力最强,那么等质量的上述物质中该物质生成的二氧化碳最多.
解答:解:上述四种物质分别与盐酸反应,这四种物质与盐酸的质量比关系如下:
MgCO3+2HCl=MgCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑
84 44 100 44
Na2CO3+2HCl=2NaCl+H2O+CO2↑ K2CO3+2HCl=2KCl+H2O+CO2↑
106 44 138 44
由上述计算可看出,要得到44份质量的二氧化碳,需要碳酸镁84份,碳酸钙100份,碳酸钠106份,碳酸钾138份,需要的碳酸镁最少,说明碳酸镁产生二氧化碳的能力最强,则相同质量的这些物质中碳酸镁与盐酸反应生成的二氧化碳最多.
故选C.
MgCO3+2HCl=MgCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑
84 44 100 44
Na2CO3+2HCl=2NaCl+H2O+CO2↑ K2CO3+2HCl=2KCl+H2O+CO2↑
106 44 138 44
由上述计算可看出,要得到44份质量的二氧化碳,需要碳酸镁84份,碳酸钙100份,碳酸钠106份,碳酸钾138份,需要的碳酸镁最少,说明碳酸镁产生二氧化碳的能力最强,则相同质量的这些物质中碳酸镁与盐酸反应生成的二氧化碳最多.
故选C.
点评:做本类型题时若要用常规方法做的话将非常复杂,计算起来比较麻烦,我们可以从反方向进行分析,问用等质量下列各物质分别与足量稀盐酸反应后,生成CO2量最多的是哪一种,我们可以将问题转化为:得到等质量的二氧化碳哪一种物质用的最少.

练习册系列答案
相关题目
某样品为Cu和CuO的混合物,为测定样品中CuO的含量,甲、乙、丙、丁四位学生用同一种样品分别进行实验,测得的数据如下表:
| 物 质 质 量 学 生 | 甲 | 乙 | 丙 | 丁 |
| 所取固体样品的质量(g) | 30 | 25 | 20 | 20 |
| 加入硫酸溶液的质量(g) | 100 | 100 | 100 | 120 |
| 反应后剩余固体的质量(g) | 22 | 17 | 12 | 12 |
分析实验数据,回答下列问题:
⑴写出氧化铜与硫酸反应的化学方程式
⑵求混合物中氧化铜的质量分数。
⑶求硫酸溶液中溶质的质量分数。


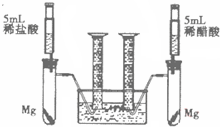 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

