题目内容
根据化学方程式A+2NaOH=B+H2O,推断B和A的相对分子质量相差
- A.18
- B.22
- C.62
- D.80
C
分析:根据质量守恒定律,参加反应的各物质的质量总和应等于生成的各物质的质量总和,所以参加反应的A和NaOH的质量和等于生成的B和H2O质量和,就可以推断B和A的相对分子质量之差.
解答:由方程式知参加反应的A和NaOH的质量和等于生成的B和H2O质量和,NaOH的相对分子质量为40,
H2O的相对分子质量为18,则A的相对分子质量+2×40=B的相对分子质量+18,推断B和A的相对分子质量相差:62
故选C.
点评:解答此题的关键是要理解质量守恒定律,并且要注意根据方程式找各物质的质量关系时要注意相对分子质量需乘以化学计量数.
分析:根据质量守恒定律,参加反应的各物质的质量总和应等于生成的各物质的质量总和,所以参加反应的A和NaOH的质量和等于生成的B和H2O质量和,就可以推断B和A的相对分子质量之差.
解答:由方程式知参加反应的A和NaOH的质量和等于生成的B和H2O质量和,NaOH的相对分子质量为40,
H2O的相对分子质量为18,则A的相对分子质量+2×40=B的相对分子质量+18,推断B和A的相对分子质量相差:62
故选C.
点评:解答此题的关键是要理解质量守恒定律,并且要注意根据方程式找各物质的质量关系时要注意相对分子质量需乘以化学计量数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图所示,A、B为实验室制取某种气体的实验装置,
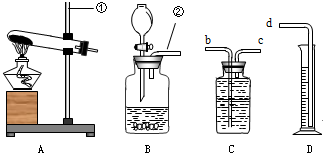
请回答下列问题:
(1)图中编号仪器的名称分别为:① ,② ;
(2)从反应物状态和反应条件来比较装置A和装置B的差异.
(3)利用装置A、C、D可粗略测定加热2g高锰酸钾所收集的氧气体积,A、C、D三装置的连接顺序是(填接口的字母):
A→ , →d.
(4)请根据化学方程式计算,2g 高锰酸钾完全分解理论上可生成标准状况下的氧气约多少升?(已知氧气在标准状况下的密度为1.429g/L).

请回答下列问题:
(1)图中编号仪器的名称分别为:①
(2)从反应物状态和反应条件来比较装置A和装置B的差异.
| 装置A | 装置B | |
| 反应物状态 | ||
| 反应条件 |
A→
(4)请根据化学方程式计算,2g 高锰酸钾完全分解理论上可生成标准状况下的氧气约多少升?(已知氧气在标准状况下的密度为1.429g/L).
 (2012?武汉)某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)
(2012?武汉)某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)