题目内容
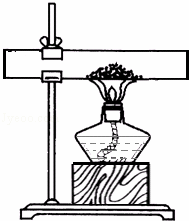
 某校课外活动小组的同学们利用水的电解实验探究水的组成,他们量取192.7mL水(水的密度为1.00g/cm3),并向水中加入了7.3g氢氧化钠固体,充分溶解后按右下图所示的装置进行实验,接通电源,当A管收集到22.3mL气体(气体密度为0.09g/L)时,停止实验.请通过计算回答:
某校课外活动小组的同学们利用水的电解实验探究水的组成,他们量取192.7mL水(水的密度为1.00g/cm3),并向水中加入了7.3g氢氧化钠固体,充分溶解后按右下图所示的装置进行实验,接通电源,当A管收集到22.3mL气体(气体密度为0.09g/L)时,停止实验.请通过计算回答:
(1)实验中B管生成的气体理论体积是______.
(2)停止实验时剩余“水中”氢氧化钠的质量分数是多少?(保留到0.01%)
解:(1)根据电解水的实验可以知道,正极和负极产生的气体的体积之比为1:2,所以可以据此求出B试管中产生的气体的体积为:22.3mL÷2=11.15mL
(2)电池负极产生的气体为氢气,其体积为:22.3mL=0.0223L
其质量为:0.0223L×0.09g/L=0.002g
设分解水的质量为x
2H2O 2H2↑+O2↑
2H2↑+O2↑
36 4
x 0.002g
 =
=
解得:x=0.018g
停止实验时剩余“水中”氢氧化钠的质量分数为: ×100%=3.65%
×100%=3.65%
答:停止实验时剩余“水中”氢氧化钠的质量分数为3.65%.
故答案为:(1)11.15mL;
(2)3.65%.
分析:(1)根据电解水的实验可以知道,正极和负极产生的气体的体积之比为1:2,所以可以据此求出B试管中产生的气体的体积;
(2)根据气体的质量结合水电解的化学方程式可以求出消耗的水的质量,然后求出氢氧化钠溶液的质量分数即可.
点评:本题对电解水实验的考查另辟蹊径,与溶质的质量分数很好结合,能较好考查出学生对知识的理解和掌握,解答时要根据相关知识细心分析.
(2)电池负极产生的气体为氢气,其体积为:22.3mL=0.0223L
其质量为:0.0223L×0.09g/L=0.002g
设分解水的质量为x

2H2O
 2H2↑+O2↑
2H2↑+O2↑ 36 4
x 0.002g
 =
=
解得:x=0.018g
停止实验时剩余“水中”氢氧化钠的质量分数为:
 ×100%=3.65%
×100%=3.65%答:停止实验时剩余“水中”氢氧化钠的质量分数为3.65%.
故答案为:(1)11.15mL;
(2)3.65%.
分析:(1)根据电解水的实验可以知道,正极和负极产生的气体的体积之比为1:2,所以可以据此求出B试管中产生的气体的体积;
(2)根据气体的质量结合水电解的化学方程式可以求出消耗的水的质量,然后求出氢氧化钠溶液的质量分数即可.
点评:本题对电解水实验的考查另辟蹊径,与溶质的质量分数很好结合,能较好考查出学生对知识的理解和掌握,解答时要根据相关知识细心分析.

练习册系列答案
相关题目
某校课外活动小组的同学欲测定某无色溶液中是否含SO42-,甲、乙两组同学分别是设计了Ⅰ、Ⅱ两个方案如下表:
为了避免犯上面两组同学相同的错误,请你设计一个实验,能确切的证明该溶液中含有SO42-,要求写明实验操作步骤、现象及结论.
| 方案 | 实验方法和步骤 | 实验现象 | 实验结论 | 老师评价 |
| Ⅰ | (1)无色溶液中加BaCl2;(2)白色沉淀中加稀HNO3 | 产生白色沉淀;沉淀不溶解 | 存在SO42- | 不合理 |
| Ⅱ | (1)无色溶液中加Ba(NO3)2;(2)白色沉淀中加稀H2SO4 | 产生白色沉淀;仍有大量白色沉淀 | 存在SO42- | 不合理 |
| 你认为 | 方案Ⅰ不合理的理由是,若溶液中有 同样有上述现象. | |||
| 方案Ⅱ不合理的理由是,若溶液中有 同样有上述现象. | ||||
 (2012?济宁)我市东部山区盛产石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析:
(2012?济宁)我市东部山区盛产石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析: 石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析:
石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析: