题目内容
配制4000g 40%的稀硫酸用以除锈,需98%的浓硫酸和水各多少毫升?(浓硫酸密度为:1.84克/毫升,水的密度为1克/毫升)
考点:有关溶质质量分数的简单计算
专题:溶液的组成及溶质质量分数的计算
分析:使用98%的浓硫酸配制40%的稀硫酸,采取加水稀释的办法完成.加水稀释时,稀释前后浓、稀溶液中的溶质质量不变.可根据这一特点建立方程解决问题.
解答:解:设需要浓硫酸的质量为x
4000g×40%=x×98%
解之得 x=
g
浓硫酸的体积=
≈887.3mL
需要水的质量=4000g-
g≈2367.3g(合2367.3mL)
答:需要98%的浓硫酸约887.3mL,水2367.3mL.
4000g×40%=x×98%
解之得 x=
| 80000 |
| 49 |
浓硫酸的体积=
| ||
| 1.84g/cm3 |
需要水的质量=4000g-
| 80000 |
| 49 |
答:需要98%的浓硫酸约887.3mL,水2367.3mL.
点评:使用溶液的溶质质量分数进行计算时,不能用溶液的体积和溶质质量分数相乘,一定要使用m=ρv的公式进行体积与质量的换算.水的密度为1g/mL,所以水的质量数(g)就可以看成其体积数(mL).

练习册系列答案
相关题目
下列鉴别CO和CO2气体的方法不正确的是( )
| A、分别通入石灰水中 |
| B、分别闻气味 |
| C、分别通入石蕊试液中 |
| D、分别伸入燃着的木条 |
从如图过氧化氢分解示意图中我们能获得许多信息,大圈代表“O”,小圈代表“H”,其中描述错误的是( )


| A、这是一个化合反应 |
| B、过氧化氢分解时原子的种类不变 |
| C、在化学变化中原子是最小的粒子 |
| D、氧分子能保持氧气的化学性质 |
某化学反应过程的微观示意图如图所示.下列说法错误的是( )


| A、原子是变化中的最小粒子 |
| B、元素的种类在化学反应前后不变 |
| C、上述反应的化学方程式可表示为:2A2+B2=2A2B |
| D、在化学变化中,分子分成原子,原子又重新组合成新的分子 |
下列净水过程发生了化学变化的是( )
| A、静置沉淀 | B、过滤 |
| C、杀菌 | D、蒸馏 |
下列粒子结构示意图中,表示阳离子的是( )
A、 |
B、 |
C、 |
D、 |
化学方程式2Mg+O2
2MgO的正确读法是( )
| ||
| A、镁加氧气等于氧化镁 |
| B、2Mg和O2等于2MgO |
| C、2个镁和1个氧气反应生成2个氧化镁 |
| D、镁在点燃的条件下,跟氧气反应生成氧化镁 |
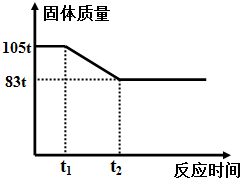 黄陂建设木兰国际广场需要一种建筑材料生石灰(主要成分是CaO).石灰公司将105吨石灰石(主要成分是CaCO3)高温煅烧,CaCO3部分分解,得到一定量的剩余固体,如图,请帮忙计算:
黄陂建设木兰国际广场需要一种建筑材料生石灰(主要成分是CaO).石灰公司将105吨石灰石(主要成分是CaCO3)高温煅烧,CaCO3部分分解,得到一定量的剩余固体,如图,请帮忙计算: