题目内容
14.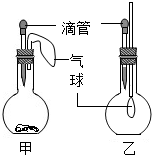 甲乙两位学生设计的实验如图所示.甲同学在烧瓶底部放入适量金属镁,乙同学在烧瓶中充满二氧化碳气体,两位同学挤压滴管分别滴入不同液体,导致两个气球均变大.请分析乙同学烧瓶里气球变大的原因是二氧化碳与氢氧化钠反应,瓶内压强减小.所发生反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.用手触摸甲同学实验的烧瓶温度明显升高,说明化学能转变成内能.
甲乙两位学生设计的实验如图所示.甲同学在烧瓶底部放入适量金属镁,乙同学在烧瓶中充满二氧化碳气体,两位同学挤压滴管分别滴入不同液体,导致两个气球均变大.请分析乙同学烧瓶里气球变大的原因是二氧化碳与氢氧化钠反应,瓶内压强减小.所发生反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.用手触摸甲同学实验的烧瓶温度明显升高,说明化学能转变成内能.
分析 根据镁能与盐酸、硫酸反应生成了气体,同时放出了热量,二氧化碳能与氢氧化钠反应生成了碳酸钠和水分析回答有关的问题.
解答 解:由题意可知,乙同学滴入的液体可能是氢氧化钠溶液,烧瓶里气球变大的原因是:二氧化碳与氢氧化钠反应,瓶内压强减小.所发生反应的化学方程式是:CO2+2NaOH═Na2CO3+H2O.甲同学滴入的可能是稀盐酸或稀硫酸,镁与酸反应生成了气体,气球胀大,用手触摸甲同学实验的烧瓶温度明显升高,说明化学能转变成内能.
故答为:二氧化碳与氢氧化钠反应,瓶内压强减小;CO2+2NaOH═Na2CO3+H2O;化学能.
点评 本题主要考查了金属二氧化碳的性质,难度不大,了解常见物质的性质是解答本题的基础知识.

练习册系列答案
相关题目
15.除去下列物质中含有的少量杂质,所选用的试剂不正确的是( )
| 序号 | 混合物 | 除杂试剂 |
| A | 一氧化碳中混有少量二氧化碳 | 足量的澄清石灰水 |
| B | 碳粉中混有少量氧化铜粉末 | 足量的稀盐酸 |
| C | 碳酸钙中混有少量氯化钠 | 足量的水 |
| D | 稀盐酸中混有少量稀硫酸 | 足量的硝酸钡溶液 |
| A. | A | B. | B | C. | C | D. | D |
2.为了对氯化钾样品(含少量KNO3)进行分析,甲、乙、丙三位同学分别进行实验,他们实验数据如表,请仔细观察和分析数据回答问题:
(1)三位同学中,哪一位同学所用氯化钾和硝酸银刚好完全反应乙(填编号)
(2)样品中氯化钾的质量分数是多少?
(3)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的溶液是只含有一种溶质的溶液?此溶液中溶质的质量分数是多少?
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量/g | 20 | 10 | 10 |
| 加入AgNO3溶液的质量/g | 100 | 100 | 150 |
| 反应后所得沉淀的质量/g | 14.35 | 14.35 | 14.35 |
(2)样品中氯化钾的质量分数是多少?
(3)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的溶液是只含有一种溶质的溶液?此溶液中溶质的质量分数是多少?
9.下列关于化学与日常生活关系的归纳中,存在错误的是( )
| A. | 化学与健康:①食用鲜黄瓜-可大量补钙 ②人体缺铁-易患贫血病 | |
| B. | 化学与生活:①减轻车内异味-开窗通风 ②防止食品受潮-用氧化钙做干燥剂 | |
| C. | 化学与安全:①重金属盐中毒-喝鲜牛奶解毒 ②煤气泄漏-关闭阀门,严禁烟火 | |
| D. | 化学与环境:①使用乙醇汽油-减少空气污染 ②合理使用农药、化肥-减少水污染 |
19.大理石广泛存在于自然界,某种大理石除主要成分CaC03外,还有少量的硫化钙.甲和乙两位同学用这种大理石和稀盐酸反应分别并展以下探究.
【查阅资料】资料一:在常温下,测的浓度均为a%的下列5种溶液的pH大小情况:
A.H2S04+2NaHC03═Na2S04+2H20+2C02↑ B.2HCl+CaS═CaCl2+H2S↑
C.C02+H20+Ca(C10)2═CaC03↓+2HClO D.H2S+CuS04═H2S04+CuS↓
资料二:常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰
【实验探究】同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
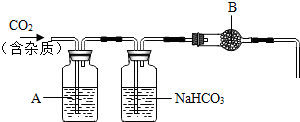
(1)制备的C02气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,A是硫酸铜溶液,饱和NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)上述装置中,B物质可能是无水氯化钙(写名称);
(4)用这个实验得到的气体测定C02的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”);
(5)乙同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
乙同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g,大理石样品纯度为83.3%.请你评价他的结论是否正确错误(填“正确”或“错误”,并简述理由)大理石中含有硫化物,硫化物与盐酸反应会生成硫化氢气体逸出,把生成的气体全部作为二氧化碳,使碳酸钙质量偏大,造成质量分数偏大.
【查阅资料】资料一:在常温下,测的浓度均为a%的下列5种溶液的pH大小情况:
| 溶质 | H2S04 | HCl | H2S | H2C03 | HClO |
| PH | 小→大 | ||||
C.C02+H20+Ca(C10)2═CaC03↓+2HClO D.H2S+CuS04═H2S04+CuS↓
资料二:常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰
【实验探究】同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:

(1)制备的C02气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,A是硫酸铜溶液,饱和NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)上述装置中,B物质可能是无水氯化钙(写名称);
(4)用这个实验得到的气体测定C02的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”);
(5)乙同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
| 实验步骤 | I.将适量盐酸加入烧杯中并称重 | Ⅱ.称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | Ⅲ.待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |