题目内容
【题目】某生产化肥碳酸氢铵(NH4HCO3)的企业,做了一个大型的广告(如图),该化肥主要成分是碳酸氢铵所含杂质不含氮元素,计算

(1)碳酸氢铵的相对分子质量是_________
(2)碳酸氢铵中各原子的个数比__________
(3)氮、氢、碳、氧四种元素的质量比_________
(4)碳酸氢铵中氮元素的质量分数为________(结果精确到0.1%)
(5)通过上述计算判断该广告属于_________(填“虚假”或“真实”广告);每袋化肥中最多含氮元素_______kg
(6)15.8kg的碳酸氢铵和________kg CO(NH2)2所含氮元素质量相等。
【答案】79 1:5:1:3 14:5:12:48 17.7% 虚假 8.86 6.0
【解析】
根据相对分子质量为构成分子的各原子的相对原子质量之和;根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比;碳酸氢铵中氮元素的质量分数根据化学式计算出;根据碳酸氢铵的质量和碳酸氢铵中氮元素的质量分数可以计算出碳酸氢铵中氮元素的质量化合物中某元素的质量=该化合物的质量×该元素的质量分数。
(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,碳酸氢铵的相对分子质量为14+1×4+1+12+16×3=79;
(2)1个碳酸氢铵分子是由1个氮原子、5个氢原子、1个碳原子和3个氧原子构成的,则碳酸氢铵中氮、氢、碳、氧四种原子的个数比为1:5:1:3;
(3)碳酸氢铵中氮、氢、碳、氧元素质量比为14:(1×5):12:(16×3)=14:5:12:48;
(4)碳酸氢铵中氮元素的质量分数为![]() ×100%≈17.7%;
×100%≈17.7%;
(5)碳酸氢铵中氮元素的质量分数小于24.1%,因此该广告是虚假的,原因是该化肥中含氮量不可能高于纯碳酸氢铵中氮元素的质量分数;每袋化肥中氮元素的质量为50kg×17.72%=8.86kg;
(6)若要达到同样的施肥效果即氮元素的质量相同,设需要尿素的质量为x,15.8kg×![]() ×100%=x×
×100%=x×![]() ×100%,解得:x=6.0kg,则需要买6.0kg尿素与原15.8kg碳酸氢铵所含氮元素质量相等。
×100%,解得:x=6.0kg,则需要买6.0kg尿素与原15.8kg碳酸氢铵所含氮元素质量相等。

【题目】实验室有5种白色固体,老师让化学实验小组同学鉴别这些固体.
(1)调查研究
①5种白色固体分别是:NaOH、Na2CO3、CuSO4、Ca(OH)2和NaHCO3.
②查阅资料:小组同学查阅了NaOH、Na2CO3和NaHCO3的一些性质.
性质 | NaOH | Na2CO3 | NaHCO3 |
溶解性 | 20℃时溶解度109g | 20℃时溶解度21.5g 溶解时放热 | 20℃时溶解度9.6g溶解时放热 |
加热 | 不分解 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
(2)实验探究:同学们的探究报告如下,请你帮助完成.
实验步骤 | 实验现象 | 实验结论 | |
第一步:在5支试管中分别放入少量的5种白色固体, 分别标上A、B、C、D、E,然后依次加入一定量的水并振荡. | A、C、D的溶液为无色;B的溶液为浑浊;E的溶液呈蓝色. | B是_____ E是_____ | |
第二步:向上述A、C、D溶液中分别滴加无色的酚酞溶液. | 三支试管中的酚酞溶液均变红. | 结论: _____ | |
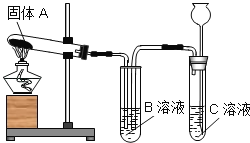
第三步:依据如图装置,对A、B、C进行实验. |
| ||
①加热固体A | B溶液无明显现象. | A是Na2CO3 | |
②待①停止加热后,通过长颈漏斗向C溶液中加入稀盐酸 | C溶液中有气泡产生,B溶液中有气泡逸出并有白色沉淀生成. | B溶液中发生反应的化学方程式为_____ | |
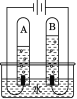
第四步:依据如图装置,对B、C进行实验. |
| 被加热的试管口有无色液滴生成,B溶液中有气泡逸出且溶液变浑浊. | C是_____ 利用排除法得出:D是NaOH |
(3)实验反思:老师引导同学们讨论了上述实验探究过程,进行全面反思,发现实验结论仍有不确定性,不能确定的物质是_____(填化学式);请用物理方法继续鉴别.
实验步骤 | 实验现象和结论 |
_____ | _____ |