题目内容
 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空:
(1)A为______极;
(2)写出电解水的化学反应方程式______.
(3)此实验的目的是______.
(4)若将质量分数为2%的NaOH溶液50g进行电解,当溶
液中NaOH的质量分数增加到4%时停止电解,则电解水的质量为______克,产生O2的物质的量为______.(请写出本题的计算过程,精确到0.1)
解:(1)与正极相连的试管生成的气体是氧气,较少.与负极相连的试管生成的是氢气,较多.氢气的体积是氧气体积的2倍.A端相连试管产生氢气多,所以A为负极.
(2)电解水能生成氢气和氧气,化学方程式为:2H2O 2H2↑+O2↑
2H2↑+O2↑
(3)电解水实验的目的是研究水的组成.
(4)设电解水的质量为x,产生氧气的物质的量为n
2%×50g=4%×(50g-x)
x=25g
被电解的水的物质的量为: =1.38mol
=1.38mol
2H2O 2H2↑+O2↑
2H2↑+O2↑
2 1
1.38mol n
 =
=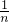
n=0.7mol
故答案为:
(1)负
(2)2H2O 2H2↑+O2↑
2H2↑+O2↑
(3)研究水的组成
(4)25g;0.7mol
分析:可以根据电解水方面的知识进行分析、判断,从而得出正确的结论.
点评:解答本题的关键是要充分理解电解水方面的内容,只有这样才能对电解水方面的知识做出正确的判断.
(2)电解水能生成氢气和氧气,化学方程式为:2H2O
 2H2↑+O2↑
2H2↑+O2↑(3)电解水实验的目的是研究水的组成.
(4)设电解水的质量为x,产生氧气的物质的量为n
2%×50g=4%×(50g-x)
x=25g
被电解的水的物质的量为:
 =1.38mol
=1.38mol 2H2O
 2H2↑+O2↑
2H2↑+O2↑2 1
1.38mol n
 =
=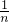
n=0.7mol
故答案为:
(1)负
(2)2H2O
 2H2↑+O2↑
2H2↑+O2↑(3)研究水的组成
(4)25g;0.7mol
分析:可以根据电解水方面的知识进行分析、判断,从而得出正确的结论.
点评:解答本题的关键是要充分理解电解水方面的内容,只有这样才能对电解水方面的知识做出正确的判断.

练习册系列答案
相关题目
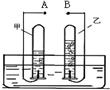 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空: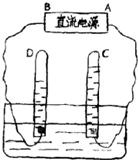 如图是电解水的实验装置图,请根据图回答:
如图是电解水的实验装置图,请根据图回答: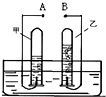 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空: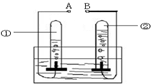 如图是电解水的实验装置图,请根据图和题意回答问题:
如图是电解水的实验装置图,请根据图和题意回答问题: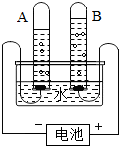 水是生命之源.请回答:
水是生命之源.请回答: