题目内容
如图所示,在托盘天平两边各放一只烧杯,调至平衡。往右边烧杯里注入一定量的稀硫酸,左边烧杯里注入相同质量的盐酸。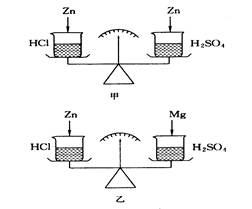
(1)两边烧杯中各投入少量相同质量的锌粒,锌粒完全溶解后,天平指针有何变化? 为什么?
(2)若左边投入锌粒,右边投相同质量的镁条,锌、镁全部溶解后,天平指针有何变化? , 为什么? 。
(1)平衡,因为两锌粒相等,生成的氢气相等。
(2)左偏,相同质量的锌、镁与足量的酸反应时,镁放出的氢气多,故左边重,指针指向左边。
解析

练习册系列答案
相关题目
下列四个实验中只需要完成三个就可以证明Fe、Cu、Ag三种金属的活动性顺序.其中不必进行的是( )
| A.将铁片放入稀盐酸 | B.将铜片放入稀盐酸 |
| C.将铁片放入硝酸银溶液 | D.将铜片放入硝酸银溶液 |
不可用来盛放硫酸铜溶液的容器是( )
| A.铜制容器 | B.瓷制容器 | C.铁制容器 | D.玻璃容器 |
设计实验判断Fe、Cu、Ag的金属活动性顺序正确的是
| A.铁丝分别放入硝酸铜溶液和硝酸银溶液 |
| B.铁丝放入硝酸铜溶液,铜丝放入硝酸银溶液 |
| C.铜丝放入硝酸亚铁溶液,铁丝放入硝酸银溶液 |
| D.银丝分别放入硝酸铜溶液和硝酸亚铁溶液 |
小明为探究金属与盐的反应,将一定质量的某种金属 M 的粉末放入 AgNO3与 Cu(NO3)2的混合溶液中,充分反应后发现,溶液呈现无色,溶液底部有少量固体粉末;过滤后在滤渣中加入适量稀盐酸,有无色气体产生。结合实际现象判断,小明得出的以下结论错误的是
| A.滤液中一定没有银离子 | B.滤渣中一定含有金属单质 M |
| C.滤渣中一定含有单质铜 | D.加入的金属 M 可能是单质铁 |
某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤液中加入适量的稀盐酸,无沉淀产生,则下列有关说法中正确的是
| A.滤液中一定含有硝酸亚铁,一定不含硝酸铜 |
| B.滤液中一定含有硝酸亚铁,可能含有硝酸银 |
| C.滤出的固体中一定含有单质银,一定没有单质铁 |
| D.滤出的固体中一定含有单质银,可能含有单质铜 |
往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,能得出的结论是
| A.滤渣中一定有Fe粉 | B.滤渣中一定有Cu粉 |
| C.滤液中一定有Fe(NO3)2 | D.滤液中一定有AgNO3、Cu(NO3)2 |
