题目内容
欲制得12.8克铜,需要用硫酸铜与多少克含杂质2%的锌反应?(反应在溶液中进行)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据锌和硫酸铜溶液反应生成铜和硫酸锌,利用铜的质量求出锌质量,进而求出含杂质2%的锌的质量即可.
解答:解:设含杂质2%的锌的质量为x
Zn+CuSO=ZnSO+Cu
65 64
x×(1-2%) 12.8g
=
x=13.3g
答:需要含杂质2%的锌13.3克
Zn+CuSO=ZnSO+Cu
65 64
x×(1-2%) 12.8g
| 65 |
| x×(1-2%) |
| 64 |
| 12.8g |
x=13.3g
答:需要含杂质2%的锌13.3克
点评:本考点考查了根据化学方程式的计算,是根据生成物的质量求反应物,是比较基础的计算题.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.题主要考查化学方程式的书写和有关化学方程式的计算,难度较小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
打开香水瓶,香气四溢,这是因为( )
| A、香水分子不断运动扩散 |
| B、香水分子变成其他物质分子 |
| C、香水分子体积变大 |
| D、香水分子发生化学变化 |
下列变化中,属于化学变化的是( )
| A、干冰升华 | B、工业制取氧气 |
| C、钢铁生锈 | D、电灯发光 |
下列物质在空气中燃烧,主要现象描述错误的是( )
| A、红磷燃烧产生大量白烟 |
| B、甲烷燃烧产生蓝色火焰 |
| C、硫燃烧产生蓝紫色火焰 |
| D、CO燃烧产生蓝色火焰 |
正确量取12mL液体,应选用的一组仪器是( )
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
| A、③④ | B、①④ | C、②④ | D、①②④ |
下列说法中正确的是( )
| A、H2的摩尔质量是2g |
| B、H2的摩尔质量是2g/mol |
| C、H2的质量是2g |
| D、1摩尔H2的质量是2g/mol |
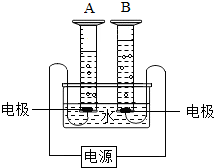 如图表示通电分解水的简易装置,回答下列问题:
如图表示通电分解水的简易装置,回答下列问题: