题目内容
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如部分数据;| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | 25 | 20 | 15 | 15 |
【答案】分析:根据表中数据分析前4次每次加入20g稀盐酸固体质量都减轻5g,说明每20g这种稀盐酸与5g碳酸钙恰好完全反应;第五次再加20g同样的稀盐酸固体质量不再减轻说明剩余的15g固体为SiO2,35g石灰石样品中碳酸钙的质量为20g,参加反应的稀盐酸质量为80g剩余20g,然后根据20g碳酸钙和80g稀盐酸反应生成的氯化钙的质量求出生成的氯化钙的质量,再求出与20g稀盐酸反应生成氯化钙的质量,与20g稀盐酸反应消耗的碳酸钙的质量为5g.然后根据溶质质量分数的计算公式计算即可.
解答:解:设35g石灰石样品全部参加反应生成的氯化钙的质量为x,生成二氧化碳的质量为a.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
20g x a
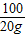 =
=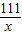
x=22.2g
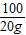 =
=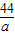
a=8.8g
设20g稀盐酸全反应生成氯化钙的质量为y,生成二氧化碳的质量为b.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
5g y b
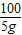 =
=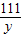
y=5.55g
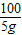 =
=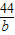
b=2.2g
与100g稀盐酸反应消耗的碳酸钙的质量为25g,所以根据质量守恒定律可知生成的氯化钙溶液的质量为125g-8.8g-2.2g=114g
所得溶液中氯化钙的质量为22.2g+5.55g=27.75g
欲将第5次实验后的溶液配成10%的CaCl2溶液,溶液的质量为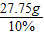 =277.5g,需要向滤液中加入水的质量为277.5g-114g=163.5g
=277.5g,需要向滤液中加入水的质量为277.5g-114g=163.5g
点评:本题主要考查学生运用化学方程式进行计算和根据溶质质量分数公式的计算能力,计算步骤繁琐只要理清题意即可计算清晰.
解答:解:设35g石灰石样品全部参加反应生成的氯化钙的质量为x,生成二氧化碳的质量为a.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
20g x a
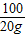 =
=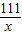
x=22.2g
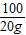 =
=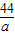
a=8.8g
设20g稀盐酸全反应生成氯化钙的质量为y,生成二氧化碳的质量为b.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
5g y b
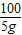 =
=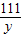
y=5.55g
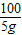 =
=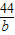
b=2.2g
与100g稀盐酸反应消耗的碳酸钙的质量为25g,所以根据质量守恒定律可知生成的氯化钙溶液的质量为125g-8.8g-2.2g=114g
所得溶液中氯化钙的质量为22.2g+5.55g=27.75g
欲将第5次实验后的溶液配成10%的CaCl2溶液,溶液的质量为
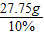 =277.5g,需要向滤液中加入水的质量为277.5g-114g=163.5g
=277.5g,需要向滤液中加入水的质量为277.5g-114g=163.5g点评:本题主要考查学生运用化学方程式进行计算和根据溶质质量分数公式的计算能力,计算步骤繁琐只要理清题意即可计算清晰.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
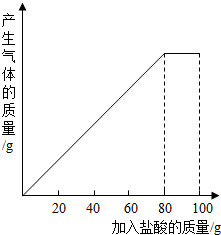 有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(2)石灰石样品中CaCO3质量分数为多少?(结果精确到0.1%)
(3)10%的CaCl2溶液可作为路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰右粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
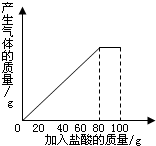 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?(结果用最简整数比表示)
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据;
欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,请计算:这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | 25 | 20 | 15 | 15 |
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不溶于水也不与盐酸反应),得到如下表部分数据.
请计算:
(1)第2次加入盐酸后,a为 g.
(2)石灰石样品中碳酸钙的质量分数为多少?
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
(4)画出35g石灰石样品中加入盐酸的质量与剩余固体的质量变化关系的示意图(在“答题卡”框图中作图)
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 | 15 | 15 |
(1)第2次加入盐酸后,a为
(2)石灰石样品中碳酸钙的质量分数为多少?
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
(4)画出35g石灰石样品中加入盐酸的质量与剩余固体的质量变化关系的示意图(在“答题卡”框图中作图)
