题目内容
13.某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究.
(1)甲同学要用KMnO4固体来制取O2,应选用上图中的A装置(填编号),该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.当O2收集满并取出集气瓶后,停止该实验的正确操作步骤是先将导管移出水面后熄灭酒精灯.
(2)查阅资料:浓盐酸具有挥发性,能挥发出氯化氢气体.
①乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色
石蕊试液变红.对这一变化的合理解释是B、C(填序号)
A.产生的CO2直接使石蕊试液变红
B.产生的CO2与水反应生成H2CO3使石蕊试液变红
C.挥发出的氯化氢溶于水使石蕊试液变红
②乙同学将制得的气体通入澄清的石灰水中,石灰水没有变浑浊,其原因是挥发出的HCl气体与石灰水反应.
(3)丙同学想用C装置制取一瓶无色无味的气体,该气体被认为最清洁的燃料,还能够还原氧化铜,则反应的化学方程式是CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.丙同学用C装置能否制取一瓶他想得到的气体,原因是否,氢气的密度比空气的密度小,不能用向上排空气法.
分析 (1)根据高锰酸钾制取氧气的反应原理书写方程式,并结合装置选择依据选择相应的装置,收集氧气完毕,要先移导管后熄灯;
(2)①烧杯中紫色石蕊试液变红,说明有酸产生,而二氧化碳、氯化氢遇酸都可以形成酸:二氧化碳与水反应生成碳酸,氯化氢溶于水形成盐酸;
②石灰水没有变浑浊,说明通入的气体不是纯净的二氧化碳;制取二氧化碳时使用具有较强挥发性的浓盐酸,因此所产生的二氧化碳中混有氯化氢气体;
(3)资源综合利用和新能源开发:最清洁的燃料----氢气,常用锌粒和硫酸进行制取,根据氢气的密度小于空气的性质选择收集方法,进行解答.
解答 解:(1)高锰酸钾制取氧气需要加热,属于“固体加热型”,所以选择A装置制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,收集氧气完毕,要先移导管后熄灯,防止水倒吸入试管,引起试管炸裂;故填:A;2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;将导管移出水面;熄灭酒精灯;
(2)①二氧化碳与水反应生成的碳酸、氯化氢气体溶于水形成的盐酸都能使石蕊试液变成红色;
故答案为:B、C;
②混在二氧化碳气体中的氯化氢气体与澄清石灰水中的氢氧化钙发生中和反应,而使气体二氧化碳不能与之发生反应,因此,澄清石灰水不能变浑浊;
故答案为:挥发出的HCl气体与石灰水反应;
(3)知“最清洁的气体燃料”为氢气,所以制取用Zn+H2SO4=ZnSO4+H2↑,因为其密度比空气的小,所以不能用向上排空气法.
故填:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;否,氢气的密度比空气的密度小,不能用向上排空气法.
点评 此题综合考查了二氧化碳和氧气的制取装置和反应原理,并联系实际,用到资源综合利用和新能源开发.

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案| A. | 洗菜、洗衣、淘米的水用来浇花、冲厕所 | |
| B. | 提倡使用节水器具 | |
| C. | 将活性炭放入硬水中使其软化 | |
| D. | 工业用水重复使用 |
 在氧气制取和检验实验中.
在氧气制取和检验实验中.(1)利用如图装置制取氧气,是通过分解过氧化氢进行的,待集气瓶中的水排完以后,应当在水下盖上玻璃片,小心地把集气瓶移出水槽,正方在桌面上.
(2)为了探究“铁丝燃烧是否需要纯氧”,采取了以下实验步骤:取5只100毫升集气瓶,标为A、B、C、D、E,分别收集体积分数为80%、70%、65%、60%和55%的氧气,进行铁丝在氧气中燃烧实验时,要在瓶内预留一定量的水,这样做的目的是防止高温熔化物溅落炸裂瓶底.为了统一标准,每瓶都预留10毫升的水,那么,氧气体积分数80%的A瓶收集氧气前应留的水的体积是77.2毫升.(已知在空气中氧气的体积分数是21%)实验现象如下表.
| 集气瓶标号 | A | B | C | D | E |
| 氧气体积分数(%) | 80 | 70 | 65 | 60 | 55 |
| 铁丝燃烧状况 | 燃烧剧烈 | 燃烧较剧烈 | 燃烧不剧烈 | 燃烧较微弱 | 不燃烧,发红 |

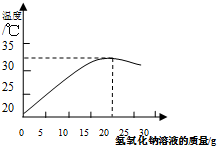 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(已知氢氧化钠与盐酸反应会放出热量)