题目内容
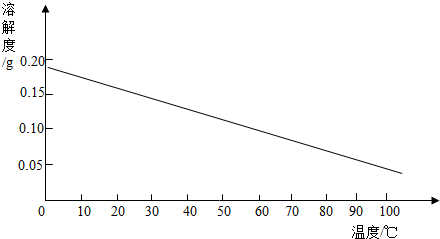
15.回顾氢氧化钙的溶解度曲线,碱溶液的溶解度越大,碱性越强.(1)从微观上说明碱具有相似化学性质的原因水溶液中都含有氢氧根离子.
(2)要使该物质的饱和溶液pH降低,可采取什么方法?滴加盐酸
(3)要使该物质的饱和溶液pH升高,可采取什么方法?加入氢氧化钠.
分析 (1)根据碱在水溶液中电离出的阴离子全部是氢氧根离子进行分析;
(2)二氧化碳、盐酸等物质都能和氢氧化钙反应,石灰石、氧化钙不能和氢氧化钙反应;
(3)使溶液的PH的增大可加入氢氧化钠;
解答 解:(1)在水溶液中电离出的阴离子全部是氢氧根离子的化合物是碱,所以具有相似化学性质的原因是都含有氢氧根离子;
(2)盐酸和氢氧化钙反应生成氯化钙和水,溶液的碱性减弱,pH减小.
(3)向改溶液中加入氢氧化钠使溶液的氢氧根离子质量分数增大,使溶液的PH的增大.
故答案为:(1)水溶液中都含有氢氧根离子;(2)滴加盐酸;(3)加入氢氧化钠.
点评 解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
6.某学生用托盘天平称量食盐放在,误把食盐放在右盘,而砝码放在左盘,称得食盐为21.5g(5g以下用游码).若按正确称量,该生称得的食盐质量应为( )
| A. | 20g | B. | 18.5g | C. | 21g | D. | 20.5g |
7.从环境保护的角度看,下列燃料最理想的是( )
| A. | 煤 | B. | 石油 | C. | 氢气 | D. | 天然气 |




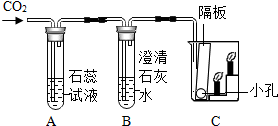 康康同学设计了如图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程式为为CO2+H2O=H2CO3;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大、不燃烧、不支持燃烧.(答出2条即可).
康康同学设计了如图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程式为为CO2+H2O=H2CO3;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大、不燃烧、不支持燃烧.(答出2条即可).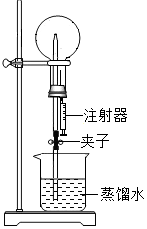 如图所示,在250mL干燥的圆底烧瓶中,充满SO2气体,并用带尖嘴导管的单孔胶塞塞紧(导管另一端的橡胶管事先用夹子夹紧),实验开始时,先将注射器中的氢氧化钠溶液推入到烧瓶中,一段时间后,打开夹子,会观察到的现象是:烧杯中的蒸馏水沿着导管进入烧瓶,形成喷泉,烧瓶中发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O,本实验成功的关键是装置不漏气.
如图所示,在250mL干燥的圆底烧瓶中,充满SO2气体,并用带尖嘴导管的单孔胶塞塞紧(导管另一端的橡胶管事先用夹子夹紧),实验开始时,先将注射器中的氢氧化钠溶液推入到烧瓶中,一段时间后,打开夹子,会观察到的现象是:烧杯中的蒸馏水沿着导管进入烧瓶,形成喷泉,烧瓶中发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O,本实验成功的关键是装置不漏气.