题目内容
化学兴趣小组用如图所示装置研究酸碱盐的性质(夹持仪器已省略).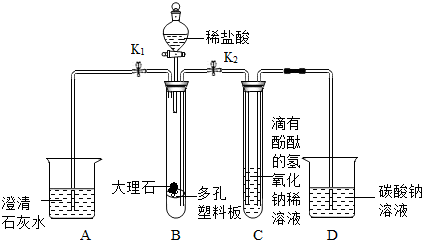
| 资料:Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应. |
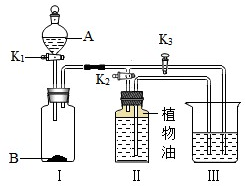
(2)当B装置中的物质仍在反应时,关闭止水夹K1,打开止水夹K2.一段时间后观察到:B装置中反应逐渐停止;C装置中溶液由红色逐渐褪为无色,此时C装置溶液中一定含有的溶质为______;D装置中液面上升,有白色沉淀生成且溶液为红色,其中液面上升的根本原因是______,此时D装置溶液中一定含有溶质NaCl,原因是______.
解:(1)用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
A中发生的反应是二氧化碳与澄清石灰水的主要成分氢氧化钙反应生成碳酸钙白色沉淀和水,方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)当B装置中的物质仍在反应时,关闭止水夹K1,二氧化碳无法排出,打开止水夹K2,则B中压强增大,会将B中液体压入到C中,氯化钙、盐酸进入C中,盐酸和C中的氢氧化钠发生反应生成氯化钠,一段时间后观察到:B装置中反应逐渐停止;C装置中溶液由红色逐渐褪为无色,说明此时溶液显中性,溶液中无氢氧化钠,则C装置溶液中一定含有的物质是:氯化钠、氯化钙、酚酞,盐酸无法判断是否含有;
D装置中液面上升,有白色沉淀生成且溶液为红色,其中液面上升的根本原因是:B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;溶液中一定含有氯化钠,是因为B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置;
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;
(2)NaCl、CaCl2、酚酞;
B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;
B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置.
分析:(1)用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;
(2)当B装置中的物质仍在反应时,关闭止水夹K1,二氧化碳无法排出,打开止水夹K2,则B中压强增大,会将B中液体压入到C中,氯化钙、盐酸进入C中,盐酸和C中的氢氧化钠发生反应生成氯化钠,一段时间后观察到:B装置中反应逐渐停止;C装置中溶液由红色逐渐褪为无色,说明此时溶液显中性,溶液中无氢氧化钠,则C装置溶液中一定含有的物质是:氯化钠、氯化钙、酚酞,盐酸无法判断是否含有;
D装置中液面上升,有白色沉淀生成且溶液为红色,其中液面上升的根本原因是:B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;溶液中一定含有氯化钠,是因为B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置.
点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,解答时,首先要分析实验装置的特点和作用,其次,了解物质的性质并结合相关知识细心分析解答即可.
A中发生的反应是二氧化碳与澄清石灰水的主要成分氢氧化钙反应生成碳酸钙白色沉淀和水,方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)当B装置中的物质仍在反应时,关闭止水夹K1,二氧化碳无法排出,打开止水夹K2,则B中压强增大,会将B中液体压入到C中,氯化钙、盐酸进入C中,盐酸和C中的氢氧化钠发生反应生成氯化钠,一段时间后观察到:B装置中反应逐渐停止;C装置中溶液由红色逐渐褪为无色,说明此时溶液显中性,溶液中无氢氧化钠,则C装置溶液中一定含有的物质是:氯化钠、氯化钙、酚酞,盐酸无法判断是否含有;
D装置中液面上升,有白色沉淀生成且溶液为红色,其中液面上升的根本原因是:B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;溶液中一定含有氯化钠,是因为B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置;
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;
(2)NaCl、CaCl2、酚酞;
B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;
B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置.
分析:(1)用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;
(2)当B装置中的物质仍在反应时,关闭止水夹K1,二氧化碳无法排出,打开止水夹K2,则B中压强增大,会将B中液体压入到C中,氯化钙、盐酸进入C中,盐酸和C中的氢氧化钠发生反应生成氯化钠,一段时间后观察到:B装置中反应逐渐停止;C装置中溶液由红色逐渐褪为无色,说明此时溶液显中性,溶液中无氢氧化钠,则C装置溶液中一定含有的物质是:氯化钠、氯化钙、酚酞,盐酸无法判断是否含有;
D装置中液面上升,有白色沉淀生成且溶液为红色,其中液面上升的根本原因是:B装置中产生CO2压强增大,将底部液体压入到C中,导致C中压强也增大,将溶液压入到D中,液面上升;溶液中一定含有氯化钠,是因为B中CaCl2通过C部分进入D装置中与Na2CO3反应生成NaCl;B装置中稀盐酸进入C装置和NaOH反应生成NaCl,部分进入D装置.
点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,解答时,首先要分析实验装置的特点和作用,其次,了解物质的性质并结合相关知识细心分析解答即可.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
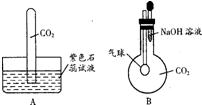 28、某化学兴趣小组用如图所示的装置做有关CO2气体的实验:
28、某化学兴趣小组用如图所示的装置做有关CO2气体的实验: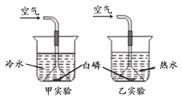
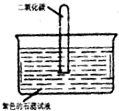 某化学兴趣小组用如图所示的装置做有关CO2气体的实验:某同学将收集满CO2气体的试管倒插入紫色石蕊试液,并轻轻振荡试管.
某化学兴趣小组用如图所示的装置做有关CO2气体的实验:某同学将收集满CO2气体的试管倒插入紫色石蕊试液,并轻轻振荡试管.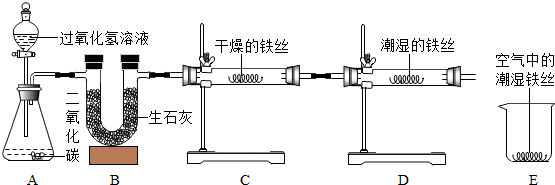
 (2013?昌平区一模)化学兴趣小组用如图所示装置研究两个问题:
(2013?昌平区一模)化学兴趣小组用如图所示装置研究两个问题: