题目内容
氨碱法制纯碱的两个主要反应的化学方程式有 和 ,主要优点有 ,我国科学家 在氨碱法的基础上发明了联合制碱法,充分利用了原料.
考点:纯碱的制取,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:氨碱法制纯碱,主要是让NaCl、NH3、CO2和H2O尽可能多的转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).再将NaHCO3加热制取纯碱,反应生成的氨气和二氧化碳可以循环使用.我国科学家侯德榜发明了联合制碱法,据此分析回答.
解答:解:氨碱法制纯碱,主要是让NaCl、NH3、CO2和H2O尽可能多的转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).再将NaHCO3加热制取纯碱,由此可知,氨碱法制纯碱的两个主要反应的化学方程式是:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl和2NaHCO3
Na2CO3+H2O+CO2↑;主要优点有:原料经济易得,二氧化碳和氨气可以循环使用,我国科学家侯德榜在氨碱法的基础上发明了联合制碱法,充分利用了原料.
故答为:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl;2NaHCO3
Na2CO3+H2O+CO2↑;原料经济易得,二氧化碳和氨气可以循环使用,侯德榜.
| ||
故答为:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl;2NaHCO3
| ||
点评:化学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,学习中要理解掌握其生产流程、原理、反应方程式等内容

练习册系列答案
相关题目
从如图过氧化氢分解示意图中我们能获得许多信息,大圈代表“O”,小圈代表“H”,其中描述错误的是( )


| A、这是一个化合反应 |
| B、过氧化氢分解时原子的种类不变 |
| C、在化学变化中原子是最小的粒子 |
| D、氧分子能保持氧气的化学性质 |
蜡烛中含有碳元素常因燃烧不充分而产生炭颗粒,室内吸烟后,会产生难闻气体,如果在室内点一支蜡烛不久就可以减弱这种气味,这是因为( )
| A、蜡烛燃烧时消耗了氧气 |
| B、蜡烛燃烧不充分产生的炭粒有吸附作用 |
| C、蜡烛燃烧后的光照作用 |
| D、蜡烛燃烧时有CO2生成 |
化学方程式2Mg+O2
2MgO的正确读法是( )
| ||
| A、镁加氧气等于氧化镁 |
| B、2Mg和O2等于2MgO |
| C、2个镁和1个氧气反应生成2个氧化镁 |
| D、镁在点燃的条件下,跟氧气反应生成氧化镁 |
如图是温州某乳品生产厂的奶粉包装袋上的部分文字说明,根据说明判断下列说法中正确的是( ) 

| A、此奶粉是纯净物 |
| B、此奶粉中不含任何化学成分 |
| C、奶粉中的钙、铁、磷、锌指的是单质 |
| D、300 g奶粉中蛋白质的质量为75 g |
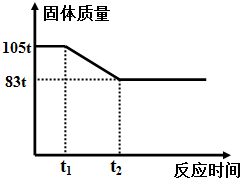 黄陂建设木兰国际广场需要一种建筑材料生石灰(主要成分是CaO).石灰公司将105吨石灰石(主要成分是CaCO3)高温煅烧,CaCO3部分分解,得到一定量的剩余固体,如图,请帮忙计算:
黄陂建设木兰国际广场需要一种建筑材料生石灰(主要成分是CaO).石灰公司将105吨石灰石(主要成分是CaCO3)高温煅烧,CaCO3部分分解,得到一定量的剩余固体,如图,请帮忙计算: