题目内容
17.以下是小意和小思两位同学解答一道计算题的实录.请你一起参与研究并完成相关问题.(计算结果精确到0.1)[题目]已知:2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑,将10g氯酸钾和2g二氧化锰混合后放入试管中加热,收集所需量的氧气后,停止加热让试管冷却,称得试管内剩余固体的质量为7.2g.求生成氯化钾的质量.
(1)小意很快得到算式:(10g+2g-7.2g),该算式所得结果是O2(填化学式)的质量,反应中生成KCl 的质量是多少?
(2)小思依据上述计算结果发现题目数据有问题.请你通过简单的计算,论证他的发现并阐明简单的理由.
分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因为化学反应中生成的气体逸出,故生成氧气的质量=参加反应前各物质的质量总和-反应后生成各物质的质量总和;根据氯酸钾分解的化学方程式和生成氧气的质量,列出比例式,就可计算出生成氯化钾的质量;
(2)剩余固体的质量=生成氯化钾的质量+二氧化锰的质量(催化剂不参与反应).
解答 解:(1)①生成氧气的质量为:10g+2g-7.2g=4.8g;
②设生成氯化钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 4.8g
$\frac{149}{x}$=$\frac{96}{4.8g}$
x=7.45g;
(2)所剩固体的质量=7.45g+2g=9.45g>7.2g,所以题目有错误.(或氯酸钾质量=7.45g+4.8g=12.25g>10g所以题目有错误.)
故答案为:(1)O2,7.45克;
(2)4.8克+7.45克=12.25克>10克,违背了质量守恒定律.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
9.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| B. | 不饱和溶液变为饱和溶液、溶质质量分数一定增大 | |
| C. | 碱性较强的溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性 | |
| D. | 活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属 |
6.下列说法正确的是( )
| A. | 镁条燃烧后生成的质量比镁条质量大,不符合质量守恒定律 | |
| B. | 水加热沸腾一段时间质量减少,符合质量守恒定律 | |
| C. | 4g碳和8g氧气完全反应生成12g二氧化碳 | |
| D. | 煤燃烧变成煤灰,质量变轻,符合质量守恒定律 |
7.在元素周期表中,硅元素如图所示,下列有关硅的说法正确的是( )


| A. | 原子序数为14 | B. | 核电荷数约为28 | ||
| C. | 相对原子质量为14 | D. | 原子质量为28.1 |
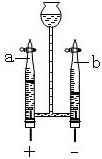 某同学制作了如图所示的简易电解水装置,进行家庭小实验(注:该装置气密性良好,且反应一段时间后停止通电)请根据要求回答问题:
某同学制作了如图所示的简易电解水装置,进行家庭小实验(注:该装置气密性良好,且反应一段时间后停止通电)请根据要求回答问题: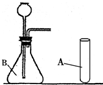 小龙同学想通过实验制取并验证二氧化碳气体.请回答下列问题:
小龙同学想通过实验制取并验证二氧化碳气体.请回答下列问题: 某同学设计了测定空气中氧气含量的实验,实验装置如图.
某同学设计了测定空气中氧气含量的实验,实验装置如图.