题目内容
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0 g该混合物粉末放入烧杯中→将140 g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图。试计算:
⑴该混合物是由铜粉和____组成的。
⑵加入105 g稀硫酸充分反应后,所得溶液的
质量。
解:(1)由第一次所加稀硫酸140g÷4=35g完全反应时,消耗金属的质=8.0g-6.8g=1.2g;
由于镁、铁、锌三种金属在反应中均呈+2价,设金属的相对原子质量为m,则
M+H2SO4═MSO4+H2↑
m 98
1.2g 35g×14%
m /1.2g ="98/" 35g×14% m=24,所以金属为镁;
⑵设生成氢气的质量为x。
Mg + H2SO4 MgSO4 + H2↑
24 2
8.0 g-4.4 g x
x="0." 3 g
所得溶液的质量:(8.0 g-4.4 g)+105 g – 0.3 g =" 108.3" g
答:略
解析

练习册系列答案
相关题目
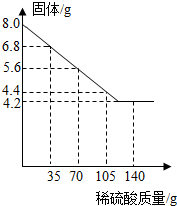 为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
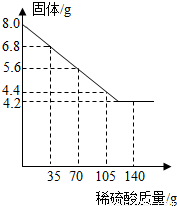 为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算: (2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
(2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算: (2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
(2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算: