题目内容
我们的生活离不开水.下列有关水的认识中错误的是( )
A. 电解水时,正极产生的气体是氢气
B. 可用肥皂水来区分硬水和软水
C. 使用无磷洗衣粉有利于保护水资源
D. 自然界中的水都是混合物
A 【解析】A、电解水时正极生成氧气负极生成氢气,错误;B、软硬水遇肥皂水的现象不同,软水泡沫丰富,硬水泡沫较少,正确;C、含磷洗衣粉对水体的污染较严重,所以使用无磷洗衣粉有利于保护水资源,正确;D、自然界中的水中含有一些可溶的和不溶的杂质,是混合物,正确。故选A。 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案某同学在课外阅读中得知:实验室用电石(主要成分CaC2)与水反应制取乙炔(C2H2)反应的方程式为CaC2+2H2O=Ca(OH)2+C2H2↑。在实验室中该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaOH
猜想二:NaOH,Ca(OH)2
猜想三:NaOH,Na2CO3
【设计并实验】
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向试管这滴入适量的碳酸钠溶液 | 猜想二不成立 | |
实验二 | 另取少量滤液于试管中,向其中加入过量稀盐酸 | 产生气泡 | 猜想 成立 |
写出实验二中产生气泡的化学方程式:
【拓展延伸】
①若向Cu(NO3)2溶液中加少量CaC2,充分反应,产生的现象是 。
②实验室保存电石应注意 。
【设计并实验】无白色沉淀生成 三 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 【拓展延伸】①有气泡产生,生成蓝色沉淀 ②密封保存 【解析】 试题分析:【设计并实验】实验一:根据反应:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,故取少量滤液于试管中,向试管这滴入适量的碳酸钠溶液,若无白色沉淀生成,则猜想二不成立 实验二:另取少量滤液于试管中,向其中加入过...某同学查资料得知,实验室常用电石(主要成分CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑(电石中的杂质不溶于水且不与水反应,也不与Na2CO3反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
(提出问题) 滤液中的成分是什么?
(猜想与假设) 猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:NaOH、Na2CO3、Ca(OH)2
你的猜想:________________。
(讨论与交流) 同学们经过讨论后一致认为猜想____是错误的,因为__________________。
为了验证猜想,同学进一步进行实验验证。
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向其中加入过量_______ | 无气泡冒出 | 猜想一不成立 |
实验二 | 另取少量滤液于试管中,向其中滴入适量的碳酸钠溶液 | ________ | 你的猜想成立,反应发生的化学方程式为____________ |
(拓展延伸) 若向CuCl2溶液中加人少量CaC2,充分反应后,可预测能够观察到的现象是________。
NaOH Ca(OH)2 三 Na2CO3与Ca(OH)2不能共存 稀盐酸 产生白色沉淀 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 产生大量气泡,并产生蓝色沉淀 【解析】根据题目信息可知:反应后滤液中一定存在的溶质是NaOH;可能存在的溶质是Ca(OH)2和Na2CO3;所以我的猜想是:NaOH和Ca(OH)2;【讨论与交流】 同学们经过讨论后一致认为猜想三是错误的,因为Na2...

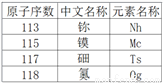
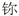 单质
单质