题目内容
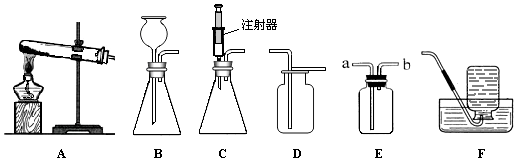
6.验室要制取一瓶纯净、干燥的二氧化碳气体,请根据以下装置回答下列问题.
(1)发生装置应选B(填写装置的字母代号).发生的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)用F装置而不用E装置收集二氧化碳的原因是二氧化碳密度比空气大,溶于水.
(3)若用G装置来收集二氧化碳,气体应从a端进入(填a或b).
(4)若要用C装置来干燥二氧化碳,C装置中应盛放的物质是浓硫酸.
(5)D装置通常用来除去二氧化碳中混有的少量氯化氢气体,请写出化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑.
(6)检查装备B的气密性方法用止水夹夹住右端管口,向长颈漏斗中加水,浸没长颈漏斗下端管口,继续加水,长颈漏斗中形成一段稳定的水柱,证明装置气密性良好.
分析 (1)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据F装置收集二氧化碳的方法是向上排空气法进行分析;
(3)根据二氧化碳密度比空气大进行分析;
(4)根据浓硫酸有吸水性进行分析;
(5)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(6)根据检验B装置气密性的正确操作方法进行分析.
解答 解:(1)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以发生装置应选B,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)F装置收集二氧化碳的方法是向上排空气法,所以用F装置而不用E装置收集二氧化碳的原因是:二氧化碳密度比空气大,溶于水;
(3)二氧化碳密度比空气大,所以用G装置来收集二氧化碳,气体应从a端进入;
(4)浓硫酸有吸水性,所以要用C装置来干燥二氧化碳,C装置中应盛放的物质是浓硫酸;
(5)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
(6)检验B装置气密性的正确操作方法是:用止水夹夹住右端管口,向长颈漏斗中加水,浸没长颈漏斗下端管口,继续加水,长颈漏斗中形成一段稳定的水柱,证明装置气密性良好.
故答案为:(1)B,CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)二氧化碳密度比空气大,溶于水;
(3)a;
(4)浓硫酸;
(5)NaHCO3+HCl=NaCl+H2O+CO2↑;
(6)用止水夹夹住右端管口,向长颈漏斗中加水,浸没长颈漏斗下端管口,继续加水,长颈漏斗中形成一段稳定的水柱,证明装置气密性良好.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| 选项 | 现象或事实 | 解释 |
| A | 金刚石和石墨的物理性质不同 | 碳原子排列方式不同 |
| B | 热胀冷缩 | 分子在不停运动 |
| C | 佝偻病和骨质疏松 | 人体中缺乏钙元素 |
| D | 用铝丝作导线 | 利用金属的导电性 |
| A. | A | B. | B | C. | C | D. | D |

| A. | t2℃时,将30ga物质加入50g水中充分搅拌,得到80ga物质的饱和溶液 | |
| B. | t1℃时,a、c两种物质的饱和溶液中所含溶质质量相等 | |
| C. | 将t2℃时三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数的大小关系是:b>a=c | |
| D. | t2℃时,若要将N点的a溶液转变为M点的a溶液,可采取恒温蒸发溶剂的方法 |
| A. | 为灭掉室内大火,迅速打开门窗降温 | |
| B. | 发现燃气泄漏,立即打开电风扇通风 | |
| C. | 为除去铝壶中的水垢,用盐酸长时间浸泡 | |
| D. | 遭遇火灾时,用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域 |
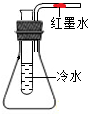 如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )| A. | 氢氧化钠固体 | B. | 生石灰 | C. | 浓硫酸 | D. | 蔗糖 |

 如图是某同学正在绘制的在实验室用混合物制取氧气的装置图
如图是某同学正在绘制的在实验室用混合物制取氧气的装置图