题目内容
某学习小组在探究“酸的化学性质”时,做了如图所示的A、B两个实验.分别向氢氧化钠和碳酸钠溶液中加入一定质量的稀硫酸,反应结束后,把废液倒入同一个废液缸中,观察到废液缸中产生少量气泡.请回答下列问题:
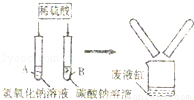
(1)试管A中的化学方程式是 ,在实验过程中并没有观察到该反应的明显现象,请你写出一种能观察到变化发生的方法 (2)通过分析废液缸中的现象,你认为B试管的废液中溶质成分是 (填化学式,下同);
(3)小组同学对废液缸中最终废液的成分进行探究,请你一起参与探究.
【提出问题】最终废液中溶质是什么?
【查阅资料】硫酸钠溶液显中性.
【假设猜想】猜想①:Na2SO4
猜想②:Na2SO4、Na2CO3
猜想③:
【实验探究】请你设计实验,确定哪个猜想是正确的.
|
实验步骤 |
|
实验结论 |
|
|
|
猜想1正确 |
|
|
猜想2正确 |
|
|
|
猜想3正确 |
(1)2NaOH+H2SO4═Na2SO4+2H2O;先在碱的溶液中滴加几滴酚酞试液,再逐滴滴加稀硫酸;(2)Na2CO3、Na2SO4;(3)【假设猜想】Na2SO4、H2SO4;【实验探究】可利用石蕊试液利用碳酸钠的溶液显碱性,稀硫酸的溶液显酸性的有关知识分析;含有硫酸的假设溶液会变红,含有碳酸钠的溶液会变蓝,只含硫酸钠的溶液石蕊不会变色;
|
实验步骤 |
实验结论 |
|
取少量废液于试管中; |
石蕊不变色 |
|
滴加紫色石蕊试液; |
石蕊试液变蓝 |
|
|
石蕊试液变红 |
【解析】
试题分析:(1)氢氧化钠和硫酸反应会生成硫酸钠和水,方程式为2NaOH+H2SO4═Na2SO4+2H2O;该反应没有现象,所以可以预先在碱的溶液中滴加几滴酚酞试液,此时溶液为红色,滴加硫酸至恰好反应红色褪去,则可以证明该反应能够进行(合理即可);(2)由于废液中会出现气泡则碳酸钠一定有剩余,且碳酸钠和稀硫酸反应一定会生成硫酸钠,所以溶液中的溶质一定是Na2CO3和Na2SO4;(3)【假设猜想】由反应的过程可知该溶液中一定有硫酸钠,且要利用碳酸钠和硫酸不会共存分析可知猜想应该存在三种情况:①只有硫酸钠;②含有硫酸钠和碳酸钠;③含有硫酸钠和硫酸;【实验探究】可利用石蕊试液利用碳酸钠的溶液显碱性,稀硫酸的溶液显酸性的有关知识分析;含有硫酸的假设溶液会变红,含有碳酸钠的溶液会变蓝,只含硫酸钠的溶液石蕊不会变色;
考点:酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式..

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案 (2012?沈阳)某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
(2012?沈阳)某学习小组在探究酸的化学性质时,做了如图所示的两个实验: (2013?湖北模拟)某学习小组在探究酸的化学性质时,做了如图所示的两个实验:?
(2013?湖北模拟)某学习小组在探究酸的化学性质时,做了如图所示的两个实验:?