题目内容
14.现有镁、稀盐酸、氧气、氢氧化钠、氯化铜,请选择上述物质写出符合下列要求的化学方程式:(1)置换反应Mg+2HCl═MgCl2+H2↑;
(2)中和反应HCl+NaOH═NaCl+H2O.
用上述一种试剂或方法除去下列物质中的杂质(括号内为杂质),用化学方程式表示.
(3)CaCl2(CaCO3)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)Cu(CuO)CuO+2HCl═CuCl2+H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)镁与稀盐酸反应生成氯化镁和氢气,属于置换反应,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑.
(2)稀盐酸与氢氧化钠反应生成氯化钠和水,属于中和反应,反应的化学方程式为:HCl+NaOH═NaCl+H2O.
(3)碳酸钙能与稀盐酸反应生成氯化钙、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(4)氧化铜能与稀盐酸反应生成氯化铜和水,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CuO+2HCl═CuCl2+H2O.
故答案为:(1)Mg+2HCl═MgCl2+H2↑;(2)HCl+NaOH═NaCl+H2O;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)CuO+2HCl═CuCl2+H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
17.日常生活中,区别下列各组物质所用的方法,正确的是( )
| A. | 白酒和白醋--观察颜色 | B. | 棉线和羊毛线--灼烧,闻气味 | ||
| C. | 黄铜和黄金--观察颜色 | D. | 食盐和苏打--加水,观察是否溶解 |
5.做家庭小实验时,下列做法错误的是( )
| A. | 用废电池中的碳棒做电极,试验氯化钠溶液的导电性 | |
| B. | 用鸡蛋壳代替石灰石与盐酸反应观察气体的生成 | |
| C. | 用过量的食醋溶液长时间浸泡铝壶出去铝壶内壁水垢 | |
| D. | 用红紫色花瓣的酒精浸出液试验石灰水和食醋的酸碱性 |
6.某兴趣小组同学为了验证铜、铁、银的金属活动性强弱,进行了如下的实验研究.
(2)实验前用砂纸打磨金属丝的目的是除去金属表面的氧化膜.
(3)实验前需要用98%的浓硫酸10ml配制10%的稀硫酸.
①用到仪器有烧杯、量筒、玻璃杯、还缺少的一种仪器是胶头滴管.
②量取蒸馏水体积时,若仰视读数,则会导致硫酸溶质质量分数<10%(填“>”、“<”或“=”).
③下列实验中,稀释浓硫酸的方法正确的是C.

(4)拓展应用:硫酸铜溶液和熟石灰混合,可制农药波尔多液.不能用铁制容器盛放波尔多液的原因是CuSO4+Fe=Cu+FeSO4(用化学方程式表示).
| 实验设计 |  |  |  |
| 实验现象 | (1)观察到现 铜丝上有银白色固体析出 | 铁丝表面有气泡产生 | 铜比表面无气泡产生 |
| 实验结论 | 金属活动性:铁>铜>银 | ||
(3)实验前需要用98%的浓硫酸10ml配制10%的稀硫酸.
①用到仪器有烧杯、量筒、玻璃杯、还缺少的一种仪器是胶头滴管.
②量取蒸馏水体积时,若仰视读数,则会导致硫酸溶质质量分数<10%(填“>”、“<”或“=”).
③下列实验中,稀释浓硫酸的方法正确的是C.

(4)拓展应用:硫酸铜溶液和熟石灰混合,可制农药波尔多液.不能用铁制容器盛放波尔多液的原因是CuSO4+Fe=Cu+FeSO4(用化学方程式表示).
4.下列实验操作中,正确的是( )
| A. | 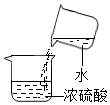 稀释浓硫酸 | B. | 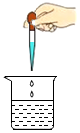 滴加液体 | C. | 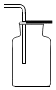 收集气体 | D. | 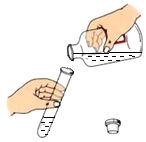 倾倒液体药品 |