题目内容
根据下列实验装置图进行氧气的制取和性质实验.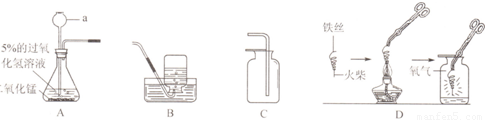
(1)仪器a的名称是______.
(2)装置A中制取氧气的反应的文字表达式为______
【答案】分析:(1)据常用仪器回答;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此书写表达式;做铁丝在氧气中燃烧的实验时集气瓶底要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,所以最好用排水法收集;
(3)铁丝末端系一根火柴的作用时引燃铁丝;实验时集气瓶炸裂了,可能的原因是:燃着的铁丝碰到集气瓶壁;
(4)可根据催化剂的定义分析解答,催化剂是改变物质的化学反应速率,而本身的质量和化学性质在反应前后保持不变,然后结合高锰酸钾受热易分解生成二氧化锰分析解答.
解答:解:(1)仪器a是用来添加液体的长颈漏斗;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此书写表达式;做铁丝在氧气中燃烧的实验时集气瓶底要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,所以最好用排水法收集;
(3)铁丝燃烧时末端系一根火柴作用是引燃铁丝;实验时集气瓶炸裂了,可能的原因是:燃着的铁丝碰到集气瓶壁,集气瓶局部骤热引起炸裂;
(4)①催化剂是化学反应前后质量和化学性质均不变的物质,该同学仅仅通过加热时氯酸钾的分解速率明显加快就判断高锰酸钾是催化剂的认识是错误的,还应验证反应前后高锰酸钾的质量和化学性质是否改变;
②高锰酸钾受热分解生成二氧化锰、锰酸钾和氧气,二氧化锰对氯酸钾的分解有催化作用,所以高锰酸钾能加快氯酸钾的分解速率;
故答案为:(1)长颈漏斗;
(2)过氧化氢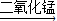 水+氧气;B;
水+氧气;B;
(3)引燃铁丝;燃着的铁丝碰到集气瓶壁;
(4)①同意;因为未验证反应前后高锰酸钾的质量和化学性质是否改变;
②因为高锰酸钾受热分解生成二氧化锰、锰酸钾和氧气,二氧化锰对氯酸钾的分解有催化作用,所以高锰酸钾能加快氯酸钾的分解速率.
点评:掌握常见实验的反应原理和实验注意事项及催化剂的定义,是解答此题的关键.
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此书写表达式;做铁丝在氧气中燃烧的实验时集气瓶底要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,所以最好用排水法收集;
(3)铁丝末端系一根火柴的作用时引燃铁丝;实验时集气瓶炸裂了,可能的原因是:燃着的铁丝碰到集气瓶壁;
(4)可根据催化剂的定义分析解答,催化剂是改变物质的化学反应速率,而本身的质量和化学性质在反应前后保持不变,然后结合高锰酸钾受热易分解生成二氧化锰分析解答.
解答:解:(1)仪器a是用来添加液体的长颈漏斗;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此书写表达式;做铁丝在氧气中燃烧的实验时集气瓶底要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,所以最好用排水法收集;
(3)铁丝燃烧时末端系一根火柴作用是引燃铁丝;实验时集气瓶炸裂了,可能的原因是:燃着的铁丝碰到集气瓶壁,集气瓶局部骤热引起炸裂;
(4)①催化剂是化学反应前后质量和化学性质均不变的物质,该同学仅仅通过加热时氯酸钾的分解速率明显加快就判断高锰酸钾是催化剂的认识是错误的,还应验证反应前后高锰酸钾的质量和化学性质是否改变;
②高锰酸钾受热分解生成二氧化锰、锰酸钾和氧气,二氧化锰对氯酸钾的分解有催化作用,所以高锰酸钾能加快氯酸钾的分解速率;
故答案为:(1)长颈漏斗;
(2)过氧化氢
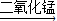 水+氧气;B;
水+氧气;B;(3)引燃铁丝;燃着的铁丝碰到集气瓶壁;
(4)①同意;因为未验证反应前后高锰酸钾的质量和化学性质是否改变;
②因为高锰酸钾受热分解生成二氧化锰、锰酸钾和氧气,二氧化锰对氯酸钾的分解有催化作用,所以高锰酸钾能加快氯酸钾的分解速率.
点评:掌握常见实验的反应原理和实验注意事项及催化剂的定义,是解答此题的关键.

练习册系列答案
相关题目







