题目内容
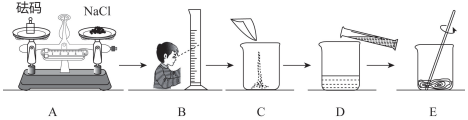
8.请根据图回答问题:
(1)实验室制取二氧化碳常选用的发生装置是C(填编号),反应方程式CaCO3+2HCl═CaCl2+H2O+CO2↑,
现需要制取2.2g二氧碳气体,需要36.5%的稀盐酸的质量为10g,反应后,要得到氯化钙固体需要用到上述的A装置(填编号).
(2)实验室用B装置(无棉花)制取氧气,所用的试剂是KClO3和MnO2,收集装置若选E,则气体应从a(填“a”或“b”)端进入,E装置内装满水收集氧气,还可用于测定气体体积,此时氧气应由b(填“a”或“b”)进入E中;用双氧水和二氧化锰制取氧气完毕,要把二氧化锰从浊液中分离出来,应选用装置D(填编号).
(3)某微型实验装置如G,该装置相当于上图装置中的B(填编号).
分析 (1)根据反应物的状态与反应的条件来确定制取装置,根据化学反应的原理来书写化学方程式、根据化学方程式进行计算、根据结晶的方法来分析;
(2)根据装置的特点确定制取原理、根据氧气的密度来分析、根据分离混合物的方法来分析;
(3)根据装置特点及所用反应物分析解答.
解答 解:(1)实验室制取二氧化碳常用固态的大理石或石灰石与液态的稀盐酸在常温下反应,所以选择装置C;大理石或石灰石的主要成分是碳酸钙,与盐酸反应生成氯化钙、水和二氧化碳;
设制取2.2g二氧碳气体,需要36.5%的稀盐酸的质量为x,则
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
36.5%x 2.2g
$\frac{73}{44}=\frac{36.5%x}{2.2g}$
x=10g
从氯化钙溶液中得到氯化钙晶体就需要对溶液进行的蒸发结晶.
故填:C;CaCO3+2HCl═CaCl2+H2O+CO2↑;10;A;
(2)B装置适用于固体加热制取氧气,因为试管口没有棉花团是,所以是加热氯酸钾与二氧化锰的混合物制取氧气;氧气的密度比空气大,所以用装置E来收集氧气时,氧气从长管进入;E装置内装满水收集氧气,还可用于测定气体体积,此时氧气应由短管进入,水从长管排出流入量筒内,量筒内水的体积即为氧气体积;二氧化锰是一种不溶于水的固体,若从浊液中分离出来可用过滤操作;故填:KClO3和MnO2;a;b;D;
(3)图G是用加热高锰酸钾的方法制取氧气,与装置中的B原理是一样的;故填:B.
点评 本题较综合的考查了学生对实验室制取氧气的反应原理、注意事项、常用仪器、装置选取方法等知识的掌握和应用,要加强平时知识的积累,才能结合具体情景分析解答相关问题.

| A. | 食用瘦肉等含铁食物预防缺铁性贫血 | |
| B. | 医疗上用氯化钠配制生理盐水 | |
| C. | 用二氧化碳灭火器扑灭图书、档案等物品的失火 | |
| D. | 用聚氯乙烯塑料制成食品保鲜膜 |
| A. | 玉米、食盐都能给人体提供能量 | |
| B. | 人体摄入氟元素的量过低,会引起贫血 | |
| C. | 纤维素属于糖类,但不能被人体消化吸收,故我们不需要摄入含纤维素的食物 | |
| D. | 人体缺乏维生素A,会引起夜盲症 |
| A. | 用灼烧、闻气味的方法鉴别涤纶和羊毛面料 | |
| B. | 用稀HCl鉴别NaOH溶液和Ba(OH)2溶液 | |
| C. | 用NaCl溶液鉴别AgNO3溶液和稀H2SO4 | |
| D. | 用FeCl3溶液鉴别KOH溶液和ZnSO4溶液 |
| A. | 鲜牛奶变质 | B. | 钢丝球刷碗 | C. | 酵母粉发酵 | D. | 洁厕剂除垢 |
 如图所示的甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能出现右图所示变化关系的是( )
如图所示的甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能出现右图所示变化关系的是( )
