题目内容
某同学对实验室中失去标签的石灰石样品进行纯度(样品中碳酸钙的质量分数)测定,取这种石灰石样品12.5g,加入94.4g一定质量分数的稀盐酸.充分反应后,共收集到4.4g二氧化碳气体(石灰石中的杂质 既不溶于水,也不和稀盐酸反应).求:
既不溶于水,也不和稀盐酸反应).求:
(1)石灰石样品中碳酸钙的质量分数.
(2)反应后所得溶液中溶质的质量分数.
| (1)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数; (2)利用化学反应方程式计算出溶质氯化钙的质量,溶液的质量等于碳酸钙的质量加上稀盐酸的质量减去二氧化碳的质量,最后再利用溶液的质量来计算溶质的质量分数. | |
| 解答: | 解:(1)设石灰石中碳酸钙的质量为x,生成的氯化钙的质量为y,则 CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 111 44 x y 4.4g
该样品中碳酸钙的质量分数为 答:石灰石样品中碳酸钙的质量分数80%; (2)因杂质既不溶于水,也不与其他物质反应,则溶液的质量为10g+94.4g﹣4.4g=100g,溶质的质量为11.1g, 则溶质的质量分数为 答:反应后所得溶液中溶质的质量分数为11.1%. |

练习册系列答案
相关题目
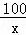 =
=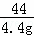 ,解得x=10g;
,解得x=10g;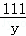 =
=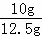 ×100%=80%;
×100%=80%;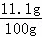 ×100%=11.1%.
×100%=11.1%.