题目内容
100g40%的氯化铵不饱和溶液,从50℃降温至10℃时,溶质的质量分数变为25%.问:从50℃降至10℃的过程中有无氯化铵晶体析出?若能析出晶体,则析出晶体质量为多少?
【答案】分析:要判断有无氯化铵晶体析出,关键是看100克40%的氯化铵不饱和溶液从50℃降温至10℃时,溶液中溶质氯化铵的质量有没有变化.如果质量减少(忽略氯化铵的挥发,因为加热至100℃时才开始显著的挥发),就有晶体析出;如果质量没变,就没有晶体析出.如果有晶体析出,那么根据溶质的质量分数关系式即可求得析出晶体的质量.
解答:解:根据溶质的质量分数= ×100%,
×100%,
可得,降温前100克40%的氯化铵不饱和溶液含溶质的质量为:
溶质的质量=溶液的质量×溶质的质量分数
=100×40%
=40(克)
先假设无晶体析出,降温后
溶质的质量=溶液的质量×溶质的质量分数
=100×25%
=25(克)
因为25<40,所以有晶体析出.
再设析出晶体x克,
根据溶质的质量分数= ×100%,
×100%,
可得25%=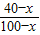 ×100%
×100%
2500-25x=4000-100x
解得x=20(克)
故答案为:有晶体析出.析出晶体20克.
点评:本题考查了溶质质量分数的计算,另外还有饱和溶液和不饱和溶液与温度的关系.在饱和溶液中,只要温度不变,溶质的质量分数就不变.解此类问题一定要注意温度对溶质质量分数的影响.将溶质的质量分数与饱和溶液结合进行一定的拓展,这也是中考命题的一个趋势.
解答:解:根据溶质的质量分数=
 ×100%,
×100%,可得,降温前100克40%的氯化铵不饱和溶液含溶质的质量为:
溶质的质量=溶液的质量×溶质的质量分数
=100×40%
=40(克)
先假设无晶体析出,降温后
溶质的质量=溶液的质量×溶质的质量分数
=100×25%
=25(克)
因为25<40,所以有晶体析出.
再设析出晶体x克,
根据溶质的质量分数=
 ×100%,
×100%,可得25%=
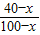 ×100%
×100%2500-25x=4000-100x
解得x=20(克)
故答案为:有晶体析出.析出晶体20克.
点评:本题考查了溶质质量分数的计算,另外还有饱和溶液和不饱和溶液与温度的关系.在饱和溶液中,只要温度不变,溶质的质量分数就不变.解此类问题一定要注意温度对溶质质量分数的影响.将溶质的质量分数与饱和溶液结合进行一定的拓展,这也是中考命题的一个趋势.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下表是氯化铵在不同温度下的溶解度:
|
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
①从表中可知:随温度升高氯化铵的溶解度 (11) 。
②60℃时,向盛有50 g水的烧杯中加入30 g氯化铵,充分搅拌,可得到氯化铵的 (12) (填“饱和”或“不饱和”)溶液,溶质的质量分数是 (13) 。
 ③A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。
③A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。
Ⅰ. C烧杯溶液中溶质的质量为 (14) g。
Ⅱ.70℃时,将A烧杯中的溶液恒温蒸发10 g溶剂后,析出a g固体,再继续恒温蒸发30g溶剂,则析出固体b克,则b克 (15) 3a 克(填“<、≤、>、≥或=”)。
Ⅲ.有关三个烧杯中溶液的说法,错误的是 (16) (填字母序号)。
a.B烧杯中溶液是不饱和溶液
b.A、B、C烧杯中的溶液在变化过程中,溶解度一定改变
c.由60℃降温至50℃时溶液质量一定减少
d.降温至60℃时,溶液中溶质质量分数一定不变
e. 降温至30℃,烧杯中一定有NH4Cl晶体析出

 温度(℃)
温度(℃)