题目内容
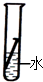
 有等质量的A、B两金属,相对原子质量A<B,将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法正确的是 ( )
有等质量的A、B两金属,相对原子质量A<B,将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法正确的是 ( )分析:根据图象可以得出:①比较氢气的多少,从而可以判断出金属的相对原子质量的大小,得到氢气多的则相对原子质量小;②判断金属的活动性强弱,反应时间短或斜线斜率大的则该金属的活动性强.
解答:解:A、金属的活动性越强的,和酸溶液反应时产生气体的速率也就越快,根据图象不难看出,金属A完全反应后所需要的时间短,即A的活动性强,故A错误;
B、由于得到的氢气一样多,根据元素的质量守恒可知,参加反应的稀盐酸和稀硫酸的溶质中氢元素的质量一定相等,又因为“将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸”,从而说明参与反应的两种酸的质量一定不一样多,故B错误;
C、由图可知“整个反应中产生的氢气的质量相等”,说法正确,故C正确;
D、由于A的相对原子质量小,因此得到相同质量的氢气,因为“相对原子质量A<B”和“在反应中A、B均为正二价”,又因为氢气的质量=
,则知参加反应的金属A的质量要少一些,故D错误;
故选C.
B、由于得到的氢气一样多,根据元素的质量守恒可知,参加反应的稀盐酸和稀硫酸的溶质中氢元素的质量一定相等,又因为“将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸”,从而说明参与反应的两种酸的质量一定不一样多,故B错误;
C、由图可知“整个反应中产生的氢气的质量相等”,说法正确,故C正确;
D、由于A的相对原子质量小,因此得到相同质量的氢气,因为“相对原子质量A<B”和“在反应中A、B均为正二价”,又因为氢气的质量=
| 金属的化合价 |
| 金属的相对原子质量 |
故选C.
点评:本题难度较大,主要考查了金属的化学性质、金属活动性顺序的应用及有关的计算,培养学生分析问题、解决问题的能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
人类的生产、生活离不开金属。
(1)用铜制电线主要是利用铜具有良好的 性。
(2)人们常用“铜墙铁壁”来形容物体的坚固。但铁在 一定条件下也能发生各种反应,
一定条件下也能发生各种反应,
如铁丝在氧气中燃烧,反应的化学方程式是________________________________。
(3)铁制品锈蚀,实际上是铁跟空气中的 发生了化学反应。防止铁制栏杆锈
蚀的一种方法是 ________________________ 。
(4)根据下 图所示回答:滤渣中一定有的金属是 ____ ,滤渣与稀硫酸反应的化学方
图所示回答:滤渣中一定有的金属是 ____ ,滤渣与稀硫酸反应的化学方
程式为_______________________________________。
 |
(5)把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的锌、铁两种金
属,反应后金属都没有剩余,产生氢气的质量随反应时间变化曲线如图。下列说法
正确的是___________。(填字母序号)
A.甲是铁,乙是锌
B.铁消耗硫酸的质量比锌大
C.参加反应的锌的质量小于铁的质量
D.充分反应后,稀硫酸一定都有剩余

 (2012?金牛区一模)如图是甲乙两种固体物质的溶解度曲线.据图回答:
(2012?金牛区一模)如图是甲乙两种固体物质的溶解度曲线.据图回答: (2013?呼和浩特)金属与我们的生活息息相关,在各个领域中用途广泛.
(2013?呼和浩特)金属与我们的生活息息相关,在各个领域中用途广泛. B、
B、 C、
C、 D、
D、