题目内容
(相对原子质量:H-1,C-12,Ca-40)某同学粗略测定家里所用白醋中醋酸的质量分数(假设白醋中的酸都看作醋酸,醋酸的化学式为CH3COOH),在玻璃杯中加入100g碳酸钙粉末,再倒入200.0g白醋.反应停止后,碳酸钙有剩余,称得玻璃杯中的固体和液体总质量为297.8g.醋酸与碳酸钙反应的化学方程式为:2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O.若不考虑醋酸与水的挥发及二氧化碳的溶解,求:
①反应生成的二氧化碳质量为______g;
②写出求溶液中醋酸质量(X)的比例式______;
③所测白醋中CH3COOH的质量分数______.
①反应生成的二氧化碳质量为______g;
②写出求溶液中醋酸质量(X)的比例式______;
③所测白醋中CH3COOH的质量分数______.
反应生成二氧化碳的质量为:200.0g+100.0g-297.8g=2.2g;
设醋酸的质量为X,
2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O
120 44
X 2.2g
=
X=
=6.0g;
所测白醋中CH3COOH的质量分数为:
×100%=3%.
答:故答案为:2.2;
=
;3%;
设醋酸的质量为X,
2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O
120 44
X 2.2g
| 120 |
| X |
| 44 |
| 2.2g |
X=
| 120×2.2g |
| 44 |
所测白醋中CH3COOH的质量分数为:
| 6.0g |
| 200.0g |
答:故答案为:2.2;
| 120 |
| X |
| 44 |
| 2.2g |

练习册系列答案
相关题目
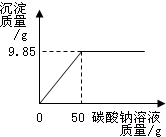
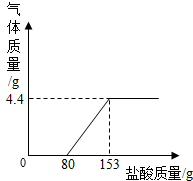 某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴滴加稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示.
某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴滴加稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示.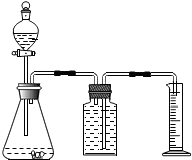 利用如图装置能制取氧气并测定所收集气体的体积.
利用如图装置能制取氧气并测定所收集气体的体积.