题目内容
硝酸铵(NH4NO3)受撞击或受热后会发生爆炸,可作炸药.又因其含氮量比较高,也可作化学肥料.试计算:
(1)100g硝酸铵中含氮元素的质量.
(2)多少克碳酸铵中的氮元素与100g硝酸铵中氮元素的质量相等?
(1)100g硝酸铵中含氮元素的质量.
(2)多少克碳酸铵中的氮元素与100g硝酸铵中氮元素的质量相等?
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据物质中某元素的质量=该物质×物质中某元素的质量分数,进行解答.
(2)利用碳酸铵与硝酸铵中氮元素的质量相等的关系进行分解答本题.
(2)利用碳酸铵与硝酸铵中氮元素的质量相等的关系进行分解答本题.
解答:解:(1)根据物质中某元素的质量=该物质×物质中某元素的质量分数,可得100g硝酸铵中含氮元素的质量为:
100g×
×100%=35g;
(2)设质量为x的碳酸铵中的氮元素与100g硝酸铵中氮元素的质量相当,可得
x×
×100%=100g×35%
则x=120g.
故答案为:120g.
100g×
| 14×2 |
| 80 |
(2)设质量为x的碳酸铵中的氮元素与100g硝酸铵中氮元素的质量相当,可得
x×
| 14×2 |
| 96 |
则x=120g.
故答案为:120g.
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
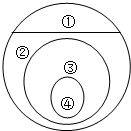 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若最大圆圈代表纯净物,下列选项正确的是( )
如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若最大圆圈代表纯净物,下列选项正确的是( )| A、①单质、③氧化物 |
| B、②化合物、④氧化物 |
| C、①单质、③化合物 |
| D、②含氧化合物、④氧化物 |
从分子的角度分析,下列解释错误的是( )
| A、好酒不怕巷子深--分子在不断运动 |
| B、海绵能吸水--分子间有空隙 |
| C、水在高温条件下生成氢气和氧气--化学变化中分子可以分成原子,原子重新组合成新分子 |
| D、热胀冷缩--分子间空隙的大小随温度的改变而改变 |
下列实验操作能达到预期目的是( )
| A、用闻气味的方法鉴别CO和CO2气体 |
| B、除去空气中的氧气又不引入新的杂质气体可用红热的木炭 |
| C、用托盘天平称取3.27g NaCl固体 |
| D、用排水法收集氧气 |
生活中的下列现象与对应的解释不相符的是( )
| A、水烧开后,壶盖被顶开--分子体积变大 |
| B、经过食堂附近,闻到饭菜香味--分子在不断运动 |
| C、50mL水和50mL酒精混合后,总体积小于100mL--分子间有间隙 |
| D、燃烧的木条伸入集满氧气的集气瓶中燃烧更旺,伸入集满二氧化碳的集气瓶中熄灭--分子不同,化学性质不同 |
海水是重要的资源,海水中约含有钠、氯、镁、钙、碘等80多种元素.这里的钠、镁、钙等指的是( )
| A、元素 | B、分子 | C、原子 | D、单质 |
 化学概念间有包含、并列、交叉等不同关系.下列选项符合图所示关系的是( )
化学概念间有包含、并列、交叉等不同关系.下列选项符合图所示关系的是( )