题目内容
5.一定质量的碳酸氢铵受热完全分解,生成了17g氨气(NH3)、18g水和44g二氧化碳,试回答下列问题:(1)碳酸氢铵是由氮 氢 氧 碳(填元素名称)组成的,其质量比为14:5:12:48;
(2)参加反应的碳酸氢铵的质量为79g.
分析 (1)根据某化肥受热分解生成氨气(NH3)、水和二氧化碳,生成物中含有的元素种类为:碳元素、氧元素、氢元素,根据质量守恒定律则可推测该物质的组成中一定含有的元素种类;
(2)根据质量守恒定律参加反应的碳酸氢铵的质量等于生成的氨气、水、二氧化碳的质量和;
解答 解:(1)由题意“某化肥受热分解生成氨气(NH3)、水和二氧化碳”,则生成物中含有的元素种类为:氮元素、碳元素、氧元素、氢元素,根据质量守恒定律和元素守恒,则可推测该物质的组成中一定含有的元素为氮元素、碳元素、氧元素、氢元素.
由碳酸氢铵的化学式(NH4HCO3)可知N、H、O、C质量比:14:1×5:12:16×3=14:5:12:48;
(2)根据质量守恒定律参加反应的碳酸氢铵的质量等于生成的氨气、水、二氧化碳的质量和;参加反应的碳酸氢铵的质量=17g+18g+44g=79g;
故答案为:(1)氮 氢 氧 碳;14:5:12:48; (2)79.
点评 本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点,有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
1.食品安全是公众普遍关注的问题,最近,“镉大米”成为公众关注的热点问题之一.据了解,含镉的大米对人的肝肾损害比较大.镉(Cd)的核电荷数为48,中子数为64,下列说法错误的是( )
| A. | 镉原子的质子数为48 | B. | 镉原子的相对原子质量为112g | ||
| C. | 镉是金属元素 | D. | 镉原子的核外电子数为48 |
2.学习化学可以了解日常生活中某些变化的本质,下列变化中属于化学变化的是( )
| A. | 钢丝球刷锅 | B. | 西瓜榨成汁 | C. | 海水晒盐 | D. | 番薯酿成酒 |

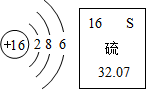 根据图示信息判断,下列说法正确的是C
根据图示信息判断,下列说法正确的是C