题目内容
1.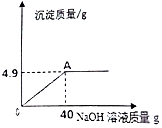 向160g硫酸铜溶液中,逐滴加入NaOH溶液,生成沉淀与加入氢氧化钠溶液的质量关系如图所示,求:
向160g硫酸铜溶液中,逐滴加入NaOH溶液,生成沉淀与加入氢氧化钠溶液的质量关系如图所示,求:(1)恰好完全反应后,所得溶液的质量为195.1g.
(2)求原硫酸铜溶液中溶质的质量分数(写出计算过程)
分析 根据给出的生成的沉淀的质量,根据化学方程式求算硫酸铜的质量,进而求算其质量分数.
解答 解:根据质量守恒可得反应后的溶液的质量为160g+40g-4.9g=195.1g
设硫酸铜的质量为x
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 98
x 4.9g
$\frac{160}{98}$=$\frac{x}{4.9g}$
x=8g
原硫酸铜溶液中溶质的质量分数为$\frac{8g}{160g}$×100%=5%
答:(1)恰好完全反应后,所得溶液的质量为 195.1g.
(2)原硫酸铜溶液中溶质的质量分数为5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
11.下列物质不需要密封保存的是( )
| A. | 浓硫酸 | B. | 石灰石 | C. | 浓氨水 | D. | 生石灰 |
12.下列实验操作中,错误的是( )
| A. |  点燃酒精灯 | B. |  检查装置气密性 | C. |  加热液体 | D. |  蒸发食盐水 |
9.下列化肥中,属于磷肥的是( )
| A. | 过磷酸钙 | B. | 氯化钾 | C. | 尿素 | D. | 氯化铵 |
6.校园里部分花草叶色发黄,易倒伏,园丁应施加的化肥是( )
| A. | KNO3 | B. | CO(NH2)2 | C. | KCl | D. | (NH4)2SO4 |
13.如图所示某原子的结构示意图,下列关于该原子的说法不正确的是( )
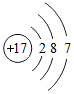

| A. | 它属于金属元素原子 | B. | 该原子有3个电子层 | ||
| C. | 该原子容易得到电子 | D. | 该原子最外层电子数为7 |
2.实验结束后,下列图示仪器处理正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
 2017年,蚌埠到怀远要修建一条轻轨线,1号线起讫点为怀远老河湾和城南客运站,线程全程36.8公里,会大大方便人们的出行和和生活,如图是轻轨图.
2017年,蚌埠到怀远要修建一条轻轨线,1号线起讫点为怀远老河湾和城南客运站,线程全程36.8公里,会大大方便人们的出行和和生活,如图是轻轨图.