题目内容
9.同学们观察了“金属材料”展台上展出的铝箔和铁丝.(1)金属能加工成“箔”或“丝”,体现了金属的延展性.
(2)铝箔光亮如新,体现了其具有抗腐蚀性,原因是4Al+3O2═2Al2O3(用化学方程式表示),而一些铁丝表面锈迹斑斑,用盐酸可以将其除去,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
(3)工业上用一氧化碳和赤铁矿炼铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据金属的物理性质,进行分析解答.
(2)根据铝在空气中能与氧气反应,其表面有一层致密的氧化铝薄膜,铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,进行分析解答.
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,进行分析解答.
解答 解:(1)金属能加工成“箔”或“丝”,是利用了金属具有良好的延展性.
(2)铝在空气中能与氧气反应,其表面有一层致密的氧化铝薄膜,反应的化学方程式为4Al+3O2═2Al2O3.
铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:(1)延展;(2)4Al+3O2═2Al2O3,Fe2O3+6HCl═2FeCl3+3H2O;(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题难度不大,掌握工业上炼铁的反应原理、金属的物理性质与化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
19.欲除去下列物质中的少量杂质,所用试剂正确的是( )
| 物质 | 杂质 | 试剂 | |
| A | CO2 | HCl气体 | NaOH溶液 |
| B | NaCl溶液 | Na2CO3 | 适量稀硫酸 |
| C | NaOH溶液 | Ca(OH)2 | 过量纯碱溶液 |
| D | CaCO3 | Na2CO3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
20. 下列粒子中,带正电的是( )
| A. | 质子 | B. | 中子 | C. | 原子 | D. | 电子 |
17.发酵粉的主要成分是碳酸氢钠,它的俗称是( )
| A. | 烧碱 | B. | 纯碱 | C. | 小苏打 | D. | 熟石灰 |
1.下列说法不符合“改善环境质量,推动绿色发展”这一主题的是( )
| A. | 垃圾分类处理 | B. | 农田过量施用农药、化肥 | ||
| C. | 工厂的废水经处理后再排放 | D. | 购物时用布袋代替塑料袋 |
18.已知某金属X与硫酸铜溶液反应的化学方程式是:X+CuSO4=Cu+XSO4,则下列说法错误的是( )
| A. | 该反应属于置换反应 | B. | 该金属的活动性比Cu强 | ||
| C. | 该金属可能是金属Al | D. | 该金属和AgNO3溶液也能发生反应 |


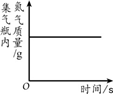


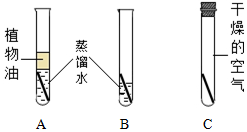 某化学课外小组通过如下实验探究铁生锈的条件.
某化学课外小组通过如下实验探究铁生锈的条件.