题目内容
某3g化合物完全燃烧,生成8.8gCO2和5.4gH2O,则该化合物中( )A.一定含有碳、氢、氧三种元素
B.只含有碳、氢两种元素
C.一定含有碳、氢元素,可能含有氧元素
D.无法确定
【答案】分析:根据题意可以知道该物质完全燃烧产生了二氧化碳和水,根据质量守恒定律可以知道,CO2中的碳元素和H2O中的氢元素都是来自于该化合物,所以可根据CO2和H2O的质量先求出碳元素和氢元素的质量,然后把碳元素和氢元素的质量之和与该化合物的质量作对比:如果等于该化合物的质量,就说明该化合物中只含有碳元素和氢元素;如果小于有机物的质量,说明有机物中含有碳、氢、氧三种元素,可以据此解答该题.
解答:解:8.8克二氧化碳中碳的质量=8.8克×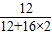 ×100%═2.4克.5.4克水中氢的质量=5.4克×
×100%═2.4克.5.4克水中氢的质量=5.4克× ×100%═0.6克.
×100%═0.6克.
综合上述分析可知,反应后氢元素和碳元素的质量之和=2.4克+0.6克=3.0克与所给的物质的质量相等,所以在该化合物中含有2种元素:氢元素、碳元素,而没有氧元素,分析所给选项可以知道选项B是正确的.
故选B.
点评:做此题首先利用的是元素守恒,即反应后有C、H、O三种元素,那么反应前也应是C、H、O三种元素;另外利用的是元素质量守恒,如反应后C元素质量和反应前C元素质量相等.只要具备了这两个守恒的思想就可以把此题做出来,属于中等难度的题.
解答:解:8.8克二氧化碳中碳的质量=8.8克×
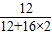 ×100%═2.4克.5.4克水中氢的质量=5.4克×
×100%═2.4克.5.4克水中氢的质量=5.4克× ×100%═0.6克.
×100%═0.6克.综合上述分析可知,反应后氢元素和碳元素的质量之和=2.4克+0.6克=3.0克与所给的物质的质量相等,所以在该化合物中含有2种元素:氢元素、碳元素,而没有氧元素,分析所给选项可以知道选项B是正确的.
故选B.
点评:做此题首先利用的是元素守恒,即反应后有C、H、O三种元素,那么反应前也应是C、H、O三种元素;另外利用的是元素质量守恒,如反应后C元素质量和反应前C元素质量相等.只要具备了这两个守恒的思想就可以把此题做出来,属于中等难度的题.

练习册系列答案
相关题目
某3g化合物完全燃烧,生成8.8gCO2和5.4gH2O,则该化合物中
| A.一定含有碳、氢、氧三种元素 |
| B.只含有碳、氢两种元素 |
| C.一定含有碳、氢元素,可能含有氧元素 |
| D.无法确定 |