题目内容
24、归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理,制取与收集方法,请你归纳出实验室制取气体反应的共同点
A.都需要加热 B.都使用催化剂 C.都没有气体作为反应物
D.原料一定只能是纯净物 E.都只生成一种气体
(2)化学上可以通过多种反应得到SO2(易溶于水,密度比空气大),例如:
①Na2SO3(固)+H2SO4═Na2SO4+SO2↑+H2O
②S+O2点燃SO2③CaSO3(固)高温CaO+SO2↑
我将选择反应

其理由是
(1)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理,制取与收集方法,请你归纳出实验室制取气体反应的共同点
C和E
(填序号).A.都需要加热 B.都使用催化剂 C.都没有气体作为反应物
D.原料一定只能是纯净物 E.都只生成一种气体
(2)化学上可以通过多种反应得到SO2(易溶于水,密度比空气大),例如:
①Na2SO3(固)+H2SO4═Na2SO4+SO2↑+H2O
②S+O2点燃SO2③CaSO3(固)高温CaO+SO2↑
我将选择反应
①
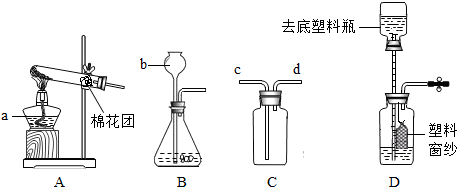
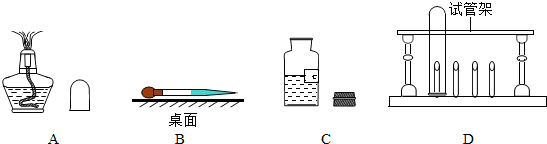
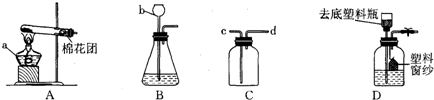
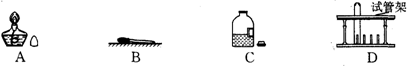
(只写一个,填序号)制取SO2.下列仪器中I的名称为水槽
.若装配该反应的发生装置,需要用上述仪器中的CH(或ABH或ABD)
(填序号),
其理由是
固体和液体反应不需要加热
.若用C、E装置组合进行SO2的收集,则SO2气体是从b
进入.(填“a”或“b”)分析:(1)总结归纳实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法;归纳出实验室制取气体反应的共同点和不同点;
(2)制取较纯净的SO2,选择实验室制取二氧化硫的反应原理;根据反应原理选择制取装置;根据“SO2(易溶于水,密度比空气大)”,选择收集装置;
(2)制取较纯净的SO2,选择实验室制取二氧化硫的反应原理;根据反应原理选择制取装置;根据“SO2(易溶于水,密度比空气大)”,选择收集装置;
解答:解:(1)总结归纳实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法;归纳出实验室制取气体反应的共同点和不同点:①需要加热;②使用催化剂;③没有气体参加反应;④原料为纯净物;⑤只生成一种气体;故相同点为:③⑤;
(2)根据实验室制取二氧化硫的反应原理,选择化学方程式为:①Na2SO3(固)+H2SO4═Na2SO4+SO2↑+H2O;根据反应物的状态和反应条件及二氧化硫的性质,因为固体和液体反应不需要加热,所以选择制取装置为:CH(或ABH或ABD);根据“二氧化硫(极易溶于水,密度比空气大)”,选择收集方法为:向上排空气法;因为密度比空气大;若用C、E装置组合进行SO2的收集,则SO2气体是从b进入.
故答为:(1)C和E;(2)①;水槽;CH(或ABH或ABD);固体和液体反应不需要加热;b
(2)根据实验室制取二氧化硫的反应原理,选择化学方程式为:①Na2SO3(固)+H2SO4═Na2SO4+SO2↑+H2O;根据反应物的状态和反应条件及二氧化硫的性质,因为固体和液体反应不需要加热,所以选择制取装置为:CH(或ABH或ABD);根据“二氧化硫(极易溶于水,密度比空气大)”,选择收集方法为:向上排空气法;因为密度比空气大;若用C、E装置组合进行SO2的收集,则SO2气体是从b进入.
故答为:(1)C和E;(2)①;水槽;CH(或ABH或ABD);固体和液体反应不需要加热;b
点评:总结归纳的方法是学习化学的重要方法;根据反应物的状态和反应条件及生成的气体的性质,选择制取装置.

练习册系列答案
相关题目